下列比较不正确的是
| A.酸性:H2SO4>H3PO4 | B.碱性:KOH>NaOH |
| C.原子半径:S<Cl | D.稳定性:NH3>CH4 |
下列有关化学用语表示正确的是( )
A.比例模型 可以表示水分子,也可以表示硫化氢分子 可以表示水分子,也可以表示硫化氢分子 |
B.电子式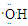 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
C.离子结构示意图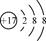 可以表示35Cl-,也可以表示37Cl 可以表示35Cl-,也可以表示37Cl |
| D.结构简式(CH3)2CHOH可以表示1-丙醇,也可以表示2-丙醇 |
向只含有Fe3+、Cu2+、H+各0.1mol及a mol SO 的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是()
的某溶液中(只来源于水电离的离子不考虑)加入足量锌粉,搅拌使其充分反应,下列说法中正确的是()
| A.当消耗13克Zn时, 得到的还原产物为0.25mol |
| B.当溶液中不再产生气泡时,溶液中大量存在的阳离子只有Zn2+ |
| C.反应中最多有两种单质生成 |
| D.反应结束时,可得到0.25molZnSO4 |
目前固体电解质在制造全固态电池及其它传感器、探测器等方面的应用日益广泛。如RbAg4I5晶体,其中迁移的离子全是Ag+。利用RbAg4I5晶体,可以制成电化学气敏传感器,下图是一种测定O2含量的气体传感器示意图。被分析的O2可以透过聚四氟乙烯薄膜,由电池电动势变化可以得知O2的含量。在气体传感器工作过程中,下列变化肯定没有发生的是
| A.I2+2Rb++2e-=2RbI | B.I2+2Ag++2e--=2AgI |
| C.Ag-e--=Ag+ | D.4AlI3+3O2==2Al2O3+6I2 |
将铁铝矾[Al2Fe(SO4)4·xH2O]溶于水中,得到浅绿色溶液,有关该溶液的叙述正确的是()
| A.铁铝矾有净水作用,其水溶液显中性 |
| B.向该溶液中加入Na2S溶液,有淡黄色沉淀 |
| C.在空气中,蒸干并灼烧该溶液,最后所得的残留固体为Al2O3、Fe2O3 |
| D.用惰性电极电解该溶液时,阴极区有沉淀。 |
取0.2mol·L-1HX溶液与0.2mol·L-1NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8(25oC),则下列说法(或关系式)正确的是()
A.混合溶液中由水电离出的c(OH-)=1×10-8mol·L-1
B.c(Na+)=c(X-)+c(HX)=0.2mol·L-1
C.c(Na+)-c(X-)=9.9×10-7mol·L-1
D.c(OH-)-c(HX)=c(H+)=1×10-6mol·L-1