(22分) 乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
(1) CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为 ;1mol O22+中含有的 键数目为 。
键数目为 。
(2)将乙炔通入[Cu(NH3)2]Cl溶液生成Cu2C2,红棕色沉淀。Cu+基态核外电子排布式为 。
(3)乙炔与氢氰酸反应可得丙烯腈 。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
。丙烯腈分子中碳原子轨道杂化类型是 ;分子中处于同一直线上的原子数目最多为 。
(4) CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中哑铃形C22-的存在,使晶胞沿一个方向拉长。CaC2晶体中1个Ca2+周围距离最近的C22-数目为 。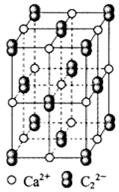
(5)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛高,其主要原因是 ;甲醛分子中碳原子的轨道杂化类型为 。
②甲醛分子的空间构型是 ;1mol甲醛分子中σ键的数目为 。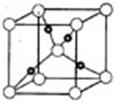
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为 。
按要求书写下列反应的离子方程式:
(1)往澄清石灰水中通入少量二氧化碳,请写出此反应的离子方程式: 。
(2)锌粒投入稀H2SO4中,溶液里氢离子的量减少,锌离子的量增加, 离子的量没有变化,反应的离子方程式是 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式: 。
(4)将过量的二氧化碳气体通入烧碱溶液中,然后将反应后的溶液分成二等份,分别加入与所得溶液溶质,等物质的量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:
① 。
② 。
现有14.4 g CO和CO2的混合气体,在标准状况下其体积为8.96 L。回答下列问题:
(1)该混合气体的平均摩尔质量为________。
(2)混合气体中碳原子的个数为________(用NA表示阿伏加德罗常数的值)。
(3)将混合气体依次通过下列如图所示装置,最后收集在气球中(实验在标准状况下测定)。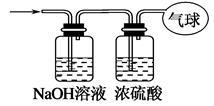
①气球中收集到的气体的摩尔质量为________。
②气球中收集到的气体中,电子总数为_____(用NA表示阿伏加德罗常数的值)。
③气球的体积为________L。
HNO3与金属反应时,还原产物可能是NO2、NO、N2O、N2和NH3中的一种或几种。某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐。在反应后的溶液中,逐滴加入4mol/L的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示。分析图像回答问题:
(1)与HNO3反应后Fe元素的化合价是 。
(2)DE段发生反应的离子方程式为: 。
(3)B点对应的沉淀的物质的量为 mol.
(4)原硝酸溶液的物质的量浓度为 mol/L.
烟气脱硫(SO2)脱硝(NOx)一体化技术是大气污染防治研究的热点。烟气中NO通常占NOx总量的90%以上,但NO的脱除难度较大。某研究小组探究用次氯酸钙溶液同时脱除烟气中SO2和NO的方法。
脱硫:Ca(ClO)2(aq) + 2SO2(g) + 2H2O(l)=CaSO4(s) + H2SO4(aq) + 2HCl(aq) Ⅰ
脱硝:3Ca(ClO)2(aq) + 4NO(g) + 2H2O(l)=3CaCl2(aq) + 4HNO3(aq) Ⅱ
请回答:
(1)脱硫过程涉及的各化学反应及其ΔH如下:
SO2(g) + H2O(l)  H2SO3(aq) ΔH=a
H2SO3(aq) ΔH=a
Ca(ClO)2(aq) + H2SO3(aq) = CaSO3(s) + 2HClO(aq) ΔH=b
CaSO3(s) + HClO(aq) = CaSO4(s) + HCl(aq) ΔH=c
H2SO3(aq) + HClO(aq) = H2SO4(aq) + HCl(aq) ΔH=d
脱硫反应Ⅰ的ΔH1= 。
(2)脱硫反应Ⅰ和脱硝反应Ⅱ的平衡常数随温度的变化如下图所示:
①判断反应Ⅱ的ΔS2 0、ΔH2 0(填<、=或>),指出有利于自发进行的温度条件是 (填“较高温度”或“较低温度”)。
②预测用次氯酸钙溶液脱硫脱硝反应进行的程度并说明理由 。
(3)与NaClO溶液吸收法相比,Ca(ClO)2法更能促进脱硫反应进行,理由是 。
(4)与NaOH溶液吸收法相比,Ca(ClO)2法的脱硫脱硝效率更高,理由是 。
一定条件下,无机物可以转化为有机物。例如,干冰与液氨反应可生成氨基甲酸铵(NH2COONH4),氨基甲酸铵受热可转化为尿素[CO(NH2)2]。新近研究发现,海底热液中有CO2和H2等无机物,还有可能通过非生物途径形成的CH4等烃类。
请回答:
(1)干冰的结构式 。
(2)干冰与液氨反应生成氨基甲酸铵的化学方程式 。
(3)氨基甲酸铵受热转化为尿素的化学方程式 。
(4)有人推测,海底热液中CH4由CO2和H2反应生成。从氧化还原反应的角度说明该推测的合理性 。
(5) 也有人推测,海底热液中的CH4由海底矿物直接生成。热液条件(如50 MPa,300 ℃)下,矿物中NaHCO3、Fe与H2O反应可生成CH4的化学方程式 。
(6)探究某矿物(xNa2CO3 ·yNaHCO3·zH2O)组成:取22.60 g试样分成两等份后进行实验。一份用酒精灯加热至恒重(270),得到固体质量为7.95 g;另一份加入足量酸,放出的气体通入过量的澄清石灰水,得到白色沉淀10.00 g。该矿物的化学式是 (用x、y、z的最简整数比表示)。
(7)BaSO4不溶于酸,若用饱和Na2CO3溶液处理可转化为溶于酸的BaCO3,沉淀转化反应的离子方程式是 。