已知烯烃有如下反应规律: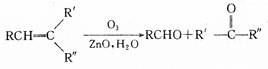 。将1mol化学式为CnH2n-4(不含C≡C和C=C=C结构)经上述方法处理后,得到的有机物和羰基(C=O)的物质的量不可能是 ( )
。将1mol化学式为CnH2n-4(不含C≡C和C=C=C结构)经上述方法处理后,得到的有机物和羰基(C=O)的物质的量不可能是 ( )
| |
A |
B |
C |
D |
| 有机物 |
1mol |
3mol |
4mol |
5mol |
| 分子中羰基 |
2mol |
4mol |
6mol |
8mol |
在日常生活中,雪碧可口可乐等饮品都是塑料容器盛装,而盛啤酒的容器却是玻璃制品,很少见到用塑料瓶盛装啤酒,这是由于塑料﹙﹚
| A.造价太高同时形成白色垃圾而引起环境污染 |
| B.太软,饮用和运输时都不方便 |
| C.相对玻璃透气性强,啤酒易被氧化而变质 |
| D.属于有机物,能与啤酒中一些成分作用不与雪碧可口可乐等饮品互溶 |
2004年神州五号飞船实现了在人航天,标志着我国航天技术达到了世界先进水平,飞船应用了许多尖端的合成材料。下列物质中不属于合成材料的是﹙﹚
| A.人造丝 | B.有机玻璃 | C.硅橡胶 | D.粘合剂 |
环境问题关系到人类的生存和发展,保护环境就是保护人类自己。从保护环境的角度出发,目前最有发展前景的一次性餐具是﹙﹚
| A.瓷器餐具 | B.塑料餐具 | C.不锈钢餐具 | D.淀粉餐具 |
下列物质一定不是天然高分子的是﹙﹚
| A.橡胶 | B.蛋白质 | C.尼龙 | D.纤维素 |
下列说法中不正确的是﹙﹚
| A.通常所说的三大合成材料是指塑料合成纤维和合成橡胶 |
| B.塑料的主要成分是合成树脂,另外还有一些添加剂 |
| C.用木材等经过加工制成的粘胶纤维属于合成纤维 |
| D.合成橡胶的原料是石油和煤 |