已知反应X + Y =" M" + N为吸热反应,对这个反应的下列说法中正确的是
| A.X的能量一定低于M的,Y的能量一定低于N的 |
| B.因为该反应为吸热反应,故一定要加热反应才能进行 |
| C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量 |
| D.X和Y的总能量一定低于M和N的总能量 |
已知:①2H2(g)+O2(g) 2H2O(g)ΔH="-483.6" kJ/mol
2H2O(g)ΔH="-483.6" kJ/mol
②H2(g)+S(g)=H2S(g) ΔH="-20.1" kJ/mol。下列判断正确的是()
| A.1 mol氢气完全燃烧吸热241.8 kJ |
| B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ |
在298 K、1.01×105 Pa下,将32 g SO2通入750 mL 1 mol/L KOH溶液中充分反应。测得反应放出x kJ的热量。已知在该条件下,1 mol SO2通入1 L 2 mol/L KOH溶液中充分反应放出y kJ的热量。则SO2与KOH溶液反应生成KHSO3的热化学方程式正确的是()
| A.SO2(g)+KOH(aq)=KHSO3(aq)ΔH="-(4x-y)" kJ/mol |
| B.SO2(g)+KOH(aq)=KHSO3(aq)ΔH="-(2x-y)" kJ/mol |
| C.SO2(g)+KOH(aq)=KHSO3(aq)ΔH="-(2y-x)" kJ/mol |
| D.2SO2(g)+2KOH(l)=2KHSO3(l)ΔH="-(8x-2y)" kJ/mol |
反应A(g)+B(g)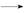 C(g) ΔH,分两步进行:①A(g)+B(g)
C(g) ΔH,分两步进行:①A(g)+B(g)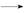 X(g) ΔH1
X(g) ΔH1
②X(g)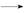 C(g) ΔH2,反应过程中能量变化如图所示,E1表示A(g)+B(g)
C(g) ΔH2,反应过程中能量变化如图所示,E1表示A(g)+B(g)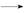 X(g)的活化能,下列说法正确的是()
X(g)的活化能,下列说法正确的是()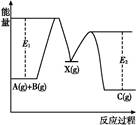
| A.ΔH1=ΔH-ΔH2>0 |
B.X(g)是反应A(g)+B(g)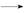 C(g)的催化剂 C(g)的催化剂 |
| C.E2是反应②的活化能 |
| D.ΔH=E1-E2 |
下列说法中错误的是()
| A.电解饱和食盐水,生成物总能量比反应物总能量高 |
| B.化学反应过程中,发生物质变化的同时一定发生能量变化 |
| C.“冰,水为之,而寒于水”,说明相同质量的水和冰,水的能量高 |
| D.食盐可用于融化冰雪,且用食盐作融雪剂不会对环境、植物生长产生任何危害 |
水热法制备纳米颗粒Y(化合物)的反应为3Fe2++2S2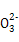 +O2+aOH-
+O2+aOH- Y+S4
Y+S4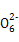 +2H2O,下列说法中,不正确的是()
+2H2O,下列说法中,不正确的是()
| A.a=4 |
| B.Y的化学式为Fe2O3 |
C.S2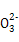 是还原剂 是还原剂 |
| D.每有1 mol O2参加反应,转移的电子为4 mol |