(21分)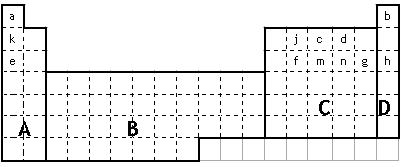
(1)在上面元素周期表中全部是金属元素的区域为 。


(a)A (b)B (c)C (d)D
(2)现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或浓硝酸中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
②甲、乙两元素相比较,金属性较强的是 (填名称),可以验证该结论的实
验是 。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
③写出甲的氧化物及氧化物对应水化物分别与强碱反应的离子方程式
、 。


(3)表中所列小写字母分别代表一种化学元素:
①m、f、j的单质熔点由高到低的顺序___________________________(填元素符号)。
②以上元素形成的金属单质中,熔点最低的是____________________(填元素符号)。
③f、m、n、g所形成的氢化物的稳定性还性由强到弱的顺序为
____________________________________________________________(填化学式);
④甲、乙、c、d、e形成的简单离子的半径由小到大的顺序为
___________________________________________________________。
⑤f元素单质是在生产中用量很大,试写出工业上制备f元素单质的化学方程式
_____________________________________________________________________。
⑥c元素的单质用途_______________________________________________(填一条)。
为了测定某饱和卤代烃的分子中卤原子的种类和数目,可按下列步骤进行实验: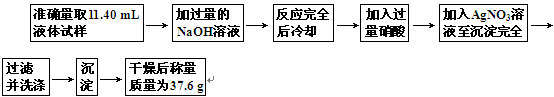
回答下列问题:
(1)准确量取11.40 mL液体所用仪器是________;
(2)加入过量硝酸的作用是__________________________________________________;
(3)加入AgNO3溶液时产生的沉淀为浅黄色,则此卤代烃中的卤原子是________;
(4)已知此卤代烃液体的密度是1.65 g/mL,其蒸气对甲烷的相对密度是11.75,则此每个卤代烃分子中卤原子的数目为________;此卤代烃的结构简式为________.
在有机反应中,反应物相同而条件不同会得到不同的主产物.下式中R代表烃基,副产物均已略去.
(请注意H和Br所加成的位置)
写出实现下列转变的各步反应的化学方程式,注意写明反应条件.
(1)由CH3CH2CH2CH2Br分两步转变为
CH3CH2CHBrCH3;
(2)由(CH3)2CHCH===CH2分两步转变为
(CH3)2CHCH2CH2OH.
C3H7Cl的结构有两种,分别为CH3CH2CH2Cl和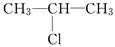
(1)CH3CH2CH2Cl在NaOH水溶液中受热反应的化学方程式是________________________________________________________________________,
反应类型为________.
(2) 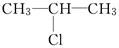 在NaOH乙醇溶液中受热反应的化学方程式是
在NaOH乙醇溶液中受热反应的化学方程式是
________________________________________________________________________,
反应类型为________.
比赛中,当运动员肌肉挫伤或扭伤时,队医随即对准运动员的受伤部位喷射药剂氯乙烷(沸点12.27℃)进行局部冷冻麻醉应急处理.乙烯和氯化氢在一定条件下制得氯乙烷的化学方程式(有机物用结构简式表示)是____________________________.该反应的类型是________反应.决定氯乙烷能用于冷冻麻醉应急处理的具体性质是___________________.
人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题:
(1)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出分子式为C6H6的一种含两个三键且无支链的链烃的结构简式________.
(2)已知分子式为C6H6的有机物有多种,其中的两种为:(Ⅰ)  、
、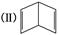 .
.
①这两种结构的区别表现在以下两方面:
定性方面(即化学性质方面):(Ⅱ)能________(填字母),而(Ⅰ)不能.
a.被高锰酸钾酸性溶液氧化 b.与溴水发生加成反应
c.与溴发生取代反应 d.与氢气发生加成反应
定量方面(即消耗反应物的量的方面):1 mol C6H6与H2加成时:(Ⅰ)需要H2________mol,而(Ⅱ)需要H2________mol.
②今发现C6H6还可能有一种如图所示的立体结构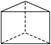 ,该结构的二氯代物有________种.
,该结构的二氯代物有________种.
(3)萘也是一种芳香烃,它的分子式是C10H8,请你判断它的结构简式可能是________(填字母).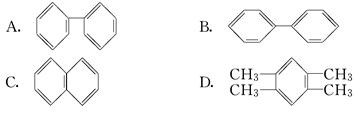
(4)现代化学认为,萘分子中碳碳键是________.