某晶体的粒子结构如图5—10所示:正六面体的8个顶点上为A粒子,12个棱的中点上为B粒子,6个面的中心上为C粒子,六面体的中心上为D粒子。那么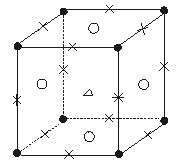
图5—10
该晶体中A、B、C、D 4种粒子的个数比为( )
A.1∶3∶3∶1 B.3∶1∶3∶1
C.1∶1∶3∶3 D.1∶3∶1∶3
同温同压下,等质量的O2和O3相比较,下列结论正确的是
| A.它们的分子数目之比是 1∶1 | B.它们的密度之比为 2∶3 |
| C.它们的体积之比是 1∶1 | D.它们的氧原子数目之比为 2∶3 |
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是
| A.2Na2O2+2H2O =4NaOH+O2↑ | B.Cl2 + H2O  HClO + HCl HClO + HCl |
| C.2F2+2H2O=4HF+O2 | D.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
下列现象或性质能体现钠的物理性质的是
①钠燃烧时发出黄色的火焰 ②钠燃烧时生成过氧化钠 ③熔点低 ④密度比水⑤热和电的良导体 ⑥钠有很强的还原性
| A.①③④⑤⑥ | B.①②③④⑤ | C.②③④⑤ | D.①③④⑤ |
下列离子方程式书写正确的是
| A.Cu(OH)2中加入硫酸:OH- + H+ = H2O |
| B.Al2(SO4)3溶液中加入足量Ba(OH)2溶液:2Al3+ + 3SO42-+ 3Ba2+ + 6OH-= 2Al(OH)3↓ + 3BaSO4↓ |
| C.钠加入水中:Na+ 2H2O= Na+ + 2OH- + H2↑ |
D.向浓盐酸中加二氧化锰:MnO2+ 4H+ + 2Cl- Mn2+ + 2H2O + Cl2↑ Mn2+ + 2H2O + Cl2↑ |
配制250 mL 0.5 mol·L-1的NaOH溶液,在下列仪器中:①量筒 ②250 mL容量瓶 ③托盘天平和砝码 ④500 mL容量瓶 ⑤烧杯 ⑥玻璃棒 ⑦漏斗 ⑧药匙 ⑨胶头滴管
⑩250 mL的烧瓶,需要用到的仪器按使用先后顺序排列正确的是
| A.⑧③⑤⑥②⑨ | B.②③⑦⑤⑥ |
| C.②⑤⑦⑥① | D.④③⑦⑤⑥ |