将ag块状碳酸钙跟足量的盐酸反应,反应物损失的质量随时间的变化曲线如图中的实线所示,在相同条件下,将bg(a>b)粉末状碳酸钙与同浓度的盐酸反应,则相应的曲线如图中的虚线所示。其中正确的是( )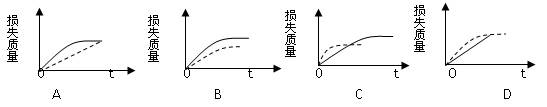
金属元素原子的最外层电子数为m,非金属元素原子的最外层电子数为n,则m与n的关系是()
| A.大于 | B.小于 | C.等于 | D.不能肯定 |
下列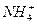 与NH3所含的质子数、核外电子数的关系描述正确的是()
与NH3所含的质子数、核外电子数的关系描述正确的是()
| A.质子数前者大于后者,核外电子数二者均相等 |
| B.质子数、核外电子数均相等 |
| C.质子数前者与后者相等,核外电子数前者小于后者 |
| D.质子数前者大于后者,核外电子数前者大于后者 |
aAm+和bBn-核外电子结构相同,则a值是()
| A.b+n+m | B.b+n-m | C.b-n-m | D.b-n+m |
某元素原子的最外层电子数为次层电子数的3倍,则该元素原子核内质子数为()
| A.3 | B.7 | C.8 | D.10 |
下列关于氢原子电子云的说法正确的是()
| A.小黑点的疏密表示电子在核外空间单位体积内的多少 |
| B.小黑点的疏密表示电子在核外空间出现机会的多少 |
| C.氢原子核外有一层带负电荷的电子 |
| D.每个小黑点表示电子在某一时刻在该空间出现一次 |