某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是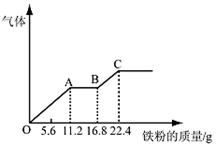
| A.原混合酸中NO3-物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由下图表示。
在下列因素中对产生H2速率有影响的是 ()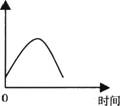
①盐酸的浓度②镁条的表面积③溶液的温度④Cl-的浓度
| A.①④ | B.③④ | C.①②③ | D.①②③④ |
下列过程中,共价键被破坏的是( )
| A.碘升华 | B.溴蒸气被活性炭吸附 |
| C.葡萄糖溶于水 | D.HCl气体溶于水 |
短周期元素A、B、C的位置如图所示,已知B、C两元素的原子序数之和是A元素的4倍,则A、B、C依次是( )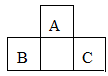
A.Be、Na、Al B.C、Al、P
C.B、Mg、Si D.O、P、Cl
已知短周期元素的离子:aAm+、bBn+、cCm-、dDn-(m>n)都具有相同的电子层结构,则下列叙述正确的是
| A.原子半径:A>B>C>D | B.离子半径:C>D>B>A |
| C.原子序数:D>C>B>A | D.单质的还原性:A>B>D>C |
下列指定微粒的个数比为2:1的是( )
| A.Be2+离子中的质子和电子 |
| B.21H原子中的中子和质子 |
| C.NaHCO3晶体中的阳离子和阴离子 |
| D.BaO2(过氧化钡)中的阴离子和阳离子 |