(14分)下面是中学化学中常用玻璃仪器组成的实验装置图(根据需要可在其中加入液体或固体)。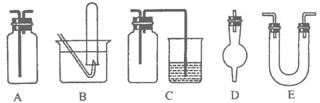
请回答下列问题:
(1)能用作干燥氨气的装置有_________(填字母);
(2)既能用于收集氯气又能用于收集一氧化氮气体的装置有_________(填字母);
(3)在氯气和铁反应实验中,能添加在制氯气和反应装置之间以除去氯气中氯化氢等杂质气体的装置有_________(填字母);
(4)能用于乙烯与溴水反应制二溴乙烷的实验装置有_________(填字母);
(5)若用C装置作二氧化硫与烧杯中氢氧化钠溶液反应的实验,则其中广口瓶的作用是_____________________________________________。
(9分)O3氧化海水中的I-是大气中碘的主要来源,将O3通入稀硫酸酸化的NaI溶液中进行模拟研究。
(1)为探究外界条件对I2生成速率的影响,做了如下三组实验,填写表中的空白处。
| 编号 |
实验目的 |
反应物 |
反应前溶液的pH |
温度 |
| 1 |
对照组 |
O3+NaI+H2SO4 |
5.2 |
25℃ |
| 2 |
①__________ |
O3+NaI+H2SO4+FeCl2 |
5.2 |
②_____ |
| 3 |
探究温度对反应速率的影响 |
O3+NaI+H2SO4 |
③_______ |
5℃ |
(2)为测定生成I2的量,用移液管取20.00mL反应后溶液于锥形瓶中,用 c mol·L-1的Na2S2O3标准液滴定,消耗V mLNa2S2O3溶液。
已知:①H2S2O3是一种弱酸;②2Na2S2O3+ I2= Na2S4O6+2NaI
①该滴定实验中除烧杯、锥形瓶外,还需要的玻璃仪器是_____________;
②该实验中可选用_______(填物质名称)作指示剂。
③反应后溶液中碘的含量为_________ g·L-1。
④甲同学认为在滴定前应微热溶液,以排除溶液中溶解的O3和O2,不然会使滴定结果偏_____(填“低”或“高”)。
如图是某研究性学习小组设计制取氯气,并以氯气为反应物进行特定反应的装置。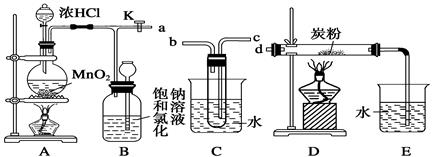
(1)要将C装置接入B和D之间,正确的接法是: a→→→d。
(2)实验开始时先点燃A处酒精灯,打开旋塞K,让Cl2充满整个装置,再点燃D处酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为。
(3)D处反应完毕后,关闭旋塞K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是,B的作用是。
(4)用量筒量取20 mL E中溶液,倒入已检查完气密性良好的分液漏斗中,然后再注入10 mL CCl4,盖好玻璃塞(如图),振荡,静置于铁架台上,等分层后取上层液和下层液,呈黄绿色的是(填“上层液”或“下层液”),再装入如图所示的烧杯中,能使有色布条褪色的是(同上)。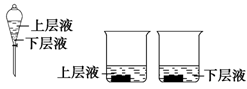
(5)在A、B、C、D、E装置中有一处需要改进,说明需要改进的理由。
将氯气用导管通入较浓的NaOH和H2O2的混合液中,在导管口与混合液的接触处有闪烁的红光出现。这是因为通气后混合液中产生的ClO-被H2O2还原,发生剧烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出。进行此实验,所用的仪器及导管如下图。
| 编号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
| 仪器及 导管 |
 |
 |
 |
 (一个) |
 (一个) |
 橡皮管 |
根据要求填写下列空白:
(1)组装氯气发生器时,应选用的仪器及导管(填写图编号)是。
(2)实验进行中,按气流方向从左到右的顺序,气体流经的各仪器及导管的编号依次是。
(3)仪器①的橡皮塞上应有个孔,原因是。
(4)实验时,仪器①中除观察到红光外还有现象。
(5)实验需用约10% H2O2溶液100 mL,现用市售30%(密度近似为1 g·cm-3)H2O2来配制,其具体配制方法是。
(6)实验时仪器①中ClO-与H2O2反应的离子方程式是。
水煤气是一种工业上常用的气体燃料,一般用焦炭和水蒸气在高温下反应制得,含有少量的CO2和水蒸气杂质。某化学兴趣小组对水煤气的主要成分进行探究。
【查阅资料】
(1)白色的无水硫酸铜粉末遇水变成蓝色;
(2)Na2CO3与少量盐酸反应生成NaHCO3和NaCl,与过量盐酸反应时生成NaCl、H2O、CO2。
【实验假设】
①可燃气体是CO;②可燃气体是H2;③可燃气体是 。
【实验过程】
实验小组按以下流程进行实验(所用试剂均为足量):
实验中,发现黑色氧化铜变红,且 ,证明水煤气含有H2;
还观察到澄清石灰水变浑浊,证明水煤气中含有另一可燃气体是 。
【实验反思】
根据实验结论,甲同学认为实验应保证安全,防止中毒。对尾气的处理方法是 。
【实验拓展】
(1)实验后,乙同学认为欲检验所用NaOH是否完全消耗,可向溶液中滴入几滴稀盐酸,若没有气体产生,则溶液中还有NaOH剩余。但丙同学认为乙同学的设计是错误的,理由是 ;
(2)丁同学通过本次实验,结合查阅的资料发现,不用任何其它试剂,只用试管和胶头滴管就可以鉴别稀盐酸和碳酸钠两种无色溶液。正确的鉴别方案及结论是 。
某校化学兴趣小组在实验室发现了一瓶标签受到腐蚀的溶液(如图),他们对该溶液是什么产生了兴趣。开始探究这瓶溶液究竟是什么?经过询问实验老师得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的一种,为了确定该药品,他们首先根据标签上残留的信息进行了分析:
(1)小明认为既然组成中含有氧元素,该溶液一定不是 溶液。
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是 。
(3)为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验:取少量样品于试管中,慢慢滴加BaCl2溶液,发现有白色沉淀产生,为了进一步检验该沉淀究竟是哪种物质,他们又向沉淀中滴加稀盐酸,结果发现沉淀溶解并产生大量气泡。由此他们得到的结论是:这瓶溶液是 ,生成沉淀的反应化学方程式为 。
(4)在总结反思本次探究活动时,小强认为这个检测实验还可简化,照样可达到目的。小强的做法是 。其理由是 。