A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如右图所示。
(1)如果A是淡黄色固体,
①写出B、E的化学式:B 、E 。
②C→D的化学方程式为_____________________。
③将足量的物质C通过入BaCl2溶液中,下列说法正确的是___________(填字母序号)。
a.溶液没有明显变化
b.溶液中出现白色浑浊
c.若继续通入Cl2或NH3,溶液都出现白色浑浊
(2)如果A是无色气体:
D→E的化学方程式为 ;
E→C的离子方程式为 。
氮可形成多种氧化物,如NO、NO2、N2O4等,NO2和N2O4可以相互转化。
(1)对反应2NO2(g) N2O4(g)△H=-57.2kJ·mol-1
N2O4(g)△H=-57.2kJ·mol-1
①在温度为T1、 T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。T1T2
(填“大于”、“小于”或“等于”);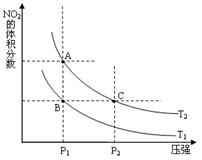
②A、C两点气体的平均相对分子质量:A C(填“ 大于”、“小”或“等于”)
大于”、“小”或“等于”)
(2)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| n(NO2)/mol |
0.40 |
n1 |
0.26 |
n3 |
n 4 |
| n(N2O4)/mol |
0.00 |
0.05 |
n 2 |
0.08 |
0.08 |
①在上述条件下,从反应开始直至20s时,二氧化氮的平均反应速率为。
②该条件下平衡常数K的值为。
③若其他条件 不变,下列既能加快正反应速率又能提高NO2转化率的措施是
不变,下列既能加快正反应速率又能提高NO2转化率的措施是
A.抽出N2O4 B.降低温度 C.加压 D.加入催化剂
④若在相同情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,
N2O4的起始的物质的量是。
⑤若其它条件不变,只将容器改为带活塞的恒压容器,
则平衡时N2O4的量0.08mol。(填“大于”、“小于”或“等于”)
能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。(注:“原子经济性”是指,在化学品合成过程中,合成方法和工艺应被设计 成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中)
成能把反应过程中所用的所有原材料尽可能多的转化到最终产物中)
(1)工业上一般采用下列两种反应合成甲醇
反应I: CO(g) + 2H2(g) CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应II: CO2(g) + 3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
上述反应符合“原子经济”原则的是:(填“I”或“Ⅱ”)。
(2)已知在常温常压下:
① 2CH3OH(l) + 3O2(g) = 2CO2(g) + 4H2O (g) ΔH =-1275.6 kJ·mol-1
(g) ΔH =-1275.6 kJ·mol-1
② 2CO (g)+ O2(g) = 2CO2(g) ΔH =-566.0 kJ·mol-1
③ H2O(g) = H2O(l)ΔH =-44.0 kJ·mol-1
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式
__________________________________________________
(3)甲醇—空气燃料电池,电解质溶液是:20%~30%的KOH溶液。请写出甲醇—空气燃料电池放电时正极的电极反应式。
。
(4)下图是一个电化学过程示意图。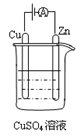
①锌片上发生的电极反应式为。
②假设使用甲醇—空气燃料电池作为本过程中的电源,铜片的质量变化96g,则燃料电池理论上需要 mol甲醇。
mol甲醇。
下图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体,F是红棕色气体。根据下图关系推断: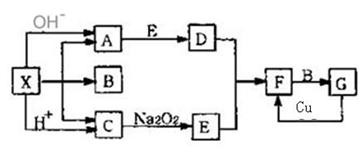
(1)化学式:X ___________。
(2) 写出C—→E的化学反应方程式______________________________________
(3) 请写出F与B反应生成G的化学方程式:____________________,该反应过程中氧化产物和还原产物的物质的量之比为__________________。
(共10分)请按要求回答下列问题:
(1)硅在无机非金属材料中一直扮演着重要角色,被誉为无机非金属材料的主角。
①下列物品用到硅单质的是;
| A.玻璃制品 | B.石英钟表 | C.计算机芯片 | D.光导纤维 E.太阳能电池 |
②硅酸盐组成复杂,往往用氧化物的形式表示,某硅酸盐其主要化学成分为Ca2Mg5Si8O22(OH)2. 把它写成氧化物的形式为:;
(2)Cl2和SO2都具有漂白性,但将这两种气体按体积比1:1通入水中得到的溶液却几乎没有漂白性,写出Cl2和SO2 1:1通入水中发生的离子反应方程式:______________________________________________________;
(3)写出二氧化硫与双氧水反应的化学方程式,并标出电子转移方向和数目: ______________________。
实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应如下:
KMnO4 + HCl(浓) → KCl + MnCl2 + Cl2↑ + H2O
(1)配平反应方程式:
KMnO4 +HCl(浓) →KCl + MnCl2 + Cl2↑ +H2O
(2)当有0.2mol电子发生转移时,生成氯气的体积(标准状况)L,被氧化的氯化氢的物质的量为 mol。该反应中HCl体现了性和性。
mol。该反应中HCl体现了性和性。