绿色化学的核心就是利用化学原理从源头上减少和清除工业生产对环境的污染。按照绿色化学的原则,最理想的“原子经济”就是反应物的原子全部转化为期望的最终产物,这时原子的利用率为 。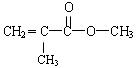 是甲基丙烯酸甲酯的结构简式。也可以写成CH2 = C(CH3)COOCH3。
是甲基丙烯酸甲酯的结构简式。也可以写成CH2 = C(CH3)COOCH3。
旧法合成它的反应是:
(CH3)2C = O+HCN (CH3)2C(OH)CN
(CH3)2C(OH)CN
(CH3)2C(OH)CN + CH3OH + H2SO4  CH2 = C(CH3)COOCH3+NH4HSO4
CH2 = C(CH3)COOCH3+NH4HSO4
新法合成它的反应是:
CH3C ≡ CH + CO + CH3OH 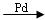 CH2= C(CH3)COOCH3
CH2= C(CH3)COOCH3
(1)与旧法相比,新法的突出优点是( )
| A.原料无爆炸危险 | B.原料都是无毒物质 |
| C.没有副产物,原子利用率高 | D.对设备腐蚀性小 |
(2)计算:甲基丙烯酸甲酯旧法合成工艺的理论上原子利用率是 。
(原子利用率=期望产物的总质量与生成物的总质量之比)
(3)写出聚甲基丙烯酸甲酯(又称有机玻璃)的结构简式 。
已知2A2(g)+B2(g) 2C3(g) △H="—akJ/mol" (a>0),在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应达平衡后,C3的浓度为w mol/L,放出热量b kJ.
2C3(g) △H="—akJ/mol" (a>0),在一个有催化剂的固定容积的容器中加入2 molA2和1 molB2,在500℃时充分反应达平衡后,C3的浓度为w mol/L,放出热量b kJ.
(1)比较a________b( 填>、=、<);
(2)若将反应温度升高到700℃,反应的平衡常数将________(增大、减小或不变);
(3)能说明该反应已经达到平衡状态的是________
a、V(C3)=2V(B2);b、容器内压强保持不变
c、V逆(A2)=2V正(B2)d、容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是________
a、及时分离出C3气体; b、适当升高温度;
c、增大B2的浓度; d、选择高效的催化剂
300℃时,将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应3A(g)+B(g) 2C (g)+2D(g) △H=Q,2min末达到平衡,生成生成0.8mol D.
2C (g)+2D(g) △H=Q,2min末达到平衡,生成生成0.8mol D.
(1)300℃时,该反应的平衡常数表达式为:K=__________________;已知K300℃<K350℃,则△H______0(填“>”或“<”)。
(2)在2min末时,B的平衡浓度为_____________,D的平均反应速率为____________;
(3)若温度不变,缩小容器容积,则A的转化率___________(填“增大”、“减小”或“不变”),原因是___________;
气态可逆反应:mA(g)+nB(g) pC (g)+qD(g),符合下图。试用“>”或“<”填(1)~(3)题。
pC (g)+qD(g),符合下图。试用“>”或“<”填(1)~(3)题。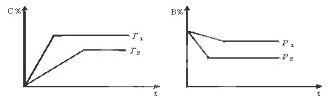
(1)温度T1___________T2,
(2)压强p1___________ p2,
(3)m+n____________ p+q,
(4)正反应为___________反应(填“放热”或“吸热”)。
25℃、101kPa时,一些物质的燃烧热为:
| 化学式 |
CO(g) |
H2(g) |
CH3OH(l) |
| △H/( kJ•mol-1) |
-283.0 |
-285.8 |
-726.5 |
请回答下列问题:
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:_____________________;
(2)根据盖斯定律完成反应的热化学方程式:CO(g)+2H2(g)═CH3OH(l)△H=_____________。
(原创)NH3是一种重要的化工产品,可用于生产尿素 [CO(NH2)2]、处理烟气等。
Ⅰ.工业上合成尿素的反应:
2NH3(g)+CO2(g) CO(NH2)2 (l) + H2O (g) ΔH
CO(NH2)2 (l) + H2O (g) ΔH
(1) 已知合成尿素的反应分两步进行:
2NH3(g)+CO2(g) NH2COONH4(s) ΔH1
NH2COONH4(s) ΔH1
NH2COONH4(s)  CO(NH2)2(l)+ H2O (g) ΔH2
CO(NH2)2(l)+ H2O (g) ΔH2
其能量变化曲线如图1所示,则△H、△H1和△H2由小到大的顺序为__________。
图1图2
(2) 某实验小组为了模拟工业上合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应:2NH3(g)+CO2(g)  CO(NH2)2 (l) + H2O (g) ,反应过程中混合气体中NH3的体积分数如图2所示。
CO(NH2)2 (l) + H2O (g) ,反应过程中混合气体中NH3的体积分数如图2所示。
①A点的逆反应速率v逆(CO2)______B点的正反应速率v正(CO2)。 (填“>”、“<”或“=”)
②下列能说明该反应达到平衡状态的是________________(填代号)。
a. NH3、CO2、H2O的分子数之比为2:1:1b.体系的压强保持不变
c.单位时间内消耗1mol CO2同时生成2mol NH3 d.2v正(NH3) =v逆(H2O)
③对于有气体参与的反应,平衡常数Kp可用气体组分(B)的平衡分压p(B)代替该气体的物质的量浓度c(B)。实验测得体系平衡时的压强为10MPa,列式计算该反应的平衡常数Kp=_______ (提示:写出Kp的表达式再代入数据进行计算,分压=总压×体积分数)。
④L(L1、L2),X可分别代表压强或温度。右图表示L一定时,该反应CO2 (g)的平衡转化率随X的变化关系。
X代表的物理量为__________。判断L1、L2的大小关系,并简述理由: 。
Ⅱ.烟气中的NOx必须脱除(即脱硝)后才能排放:
(3)下图是一种用NH3脱除烟气中 NO的原理。该脱硝反应中,氧化剂是 (填化学式) 。
(4)利用反应8NH3+6NO2═7N2+12H2O构成原电池,也能消除烟气的排放,同时还能充分利用化学能,装置如图所示。则电极b为______极;a电极的电极反应式为 。