今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g。根据上述实验,以下推测正确的是
| A.K+可能存在 | B.100 mL溶液中含0.01 mol CO32- |
| C.Cl-可能存在 | D.Ba2+一定不存在,Mg2+可能存在 |
下列A-D各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
| 甲 |
乙 |
丙 |
|
| A |
Al2O3 |
HNO3 |
Ba(OH)2 |
| B |
NH3 |
O2 |
H2SO4 |
| C |
SiO2 |
NaOH |
HF |
| D |
CO2 |
Na2O2 |
H2O |
下列表示对应化学反应的离子方程式正确的是
| A.Na2C2O4水解:C2O42-+2H2O=H2C2O4+2OH- |
| B.AgOH溶于氨水:AgOH+2NH3·H2O=[Ag(NH3)2]++OHˉ+2H2O |
| C.向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D.向酸性KMnO4溶液中通入SO2:2MnO4-+5SO2+4OH-=2Mn2++5SO42-+2H2O |
下列有关实验正确的是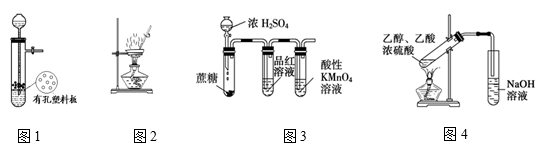
| A.图1装置用于Cu和浓H2SO4反应制取少量的SO2气体 |
| B.图2装置用于灼烧Al(OH)3 |
| C.图3装置用于检验浓硫酸与蔗糖反应产生的二氧化硫 |
| D.图4装置由于实验室制备乙酸乙酯 |
设NA为阿伏加德罗常数的值,下列说法中正确的是
| A.标准状况下,11.2 L NO和11.2 L SO3的分子总数为0.5NA |
| B.0.1molBr2与足量H2O或NaOH反应转移的电子数均为0.1NA |
| C.0.1mol的白磷(P4)或四氯化碳(CCl4)中所含的共价键数均为0.4NA |
| D.在精炼铜或电镀铜的过程中,当阴极析出铜32g转移电子数均为NA |
下列有关物质性质的应用错误的是
| A.二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸 |
| B.碳酸氢钠具有弱酸性,可用于食品发酵 |
| C.次氯酸钠具有强氧化性,可用于配制消毒液 |
| D.明矾能水解生成Al(OH)3胶体,可用作净水剂 |