( 12分)从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限。
(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于
(填选项序号)
| A.金属的导电性强弱 | B.金属在地壳中的含量多少 |
| C.金属的化合价高低 | D.金属的活动性大小 |
(2)早在西汉成书的《淮南万毕术》里,就有"曾青得铁则化为铜"的记载。曾青又有空青、白青、石胆、胆矶等名称其实都是天然的硫酸铜。
①写出"曾青得铁则化为铜"的离子方程式 。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。
正极反应
负极反应 
③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。
(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式 。
教材中引发铝热反应的试剂是 。
汽车发生强烈碰撞时,安全气囊内的NaH发生化学反应生成金属钠与氢气,所产生的气体快速充满气囊,可以达到保护车内人员的目的。
(1)请写出上述反应方程式:它的基本反应类型是
(2)若安全气囊内含有96g NaH,其物质的量为.
(3)若96g NaH完全分解,在标况下,气囊膨胀的体积约为
某溶液中只含有Na2SO4、Na2CO3和NaCl三种溶质。欲证明其中SO42-、CO32-、Cl- 三种阴离子确实存在,我们设计了如下实验,请你认真填写下面的实验报告。
| 实验步骤 |
实验现象 |
结论 |
| 1、向盛放溶液的试管中加入足量。 |
有气泡产生 |
证明有。 |
| 2、继续向试管中加入足量溶液 |
有白色沉淀生成 |
证明有。 |
| 3、过滤,向滤液中加适量的溶液 |
有白色沉淀生成 |
证明有。 |
某可逆反应从0—2分钟进行过程中, 在不同反应时间各物质的量的变化情况如下图所示。则该反应的的反应物是,生成物是,化学方程式为;反应开始至2分钟时,能否用C表示反应速率?若能,其反应速率为 _____,若不能,则其原因为 _;2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了____状态。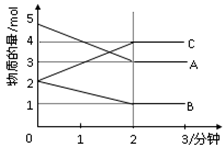
地球的表面积为5.1亿平方公里,其中海洋的面积为3.67亿平方公里,占整个地球表面积的70.8 %。海洋是一个巨大的化学资源宝库,下面是海水资源综合利用的部分流程图,请根据该图回答下列问题: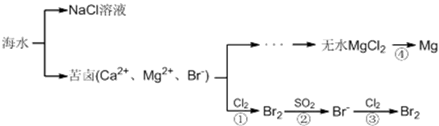
(1)淡化海水的方法有____________(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、________(填化学式),之后________(填操作名称),再加入适量________(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
(2)反应④由无水MgCl2制取金属镁的常用工业方法是__________________。
(3)向苦卤中通入Cl2置换出Br2,再用空气吹出溴并用SO2吸收,转化为Br-,反复多次,以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是_______________________。
(4)工业上也可以用Na2CO3溶液吸收吹出的Br2,生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式_________________再用H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为___________。
下表是元素周期表中的一部分,根据A~I在元素周期表中的位置,用元素符号或化学式回答下列问题:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 |
A |
|||||||
| 2 |
D |
E |
G |
I |
||||
| 3 |
B |
C |
F |
H |
(1)上表中,化学性质最不活泼的元素是_____,氧化性最强的单质是_____,还原性最强的是_____。
(2)最高价氧化物对应水化物的碱性最强的元素是________,酸性最强的元素是________。
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的是___________。
(4)请用电子式表示化合物BG的形成过程________________。
(5)写出C的最高价氧化物对应水化物与B的最高价氧化物对应水化物反应的离子方程式:______________。