某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液。请回答:
(1)浓硫酸的作用是 。
(2)球形干燥管C的作用是 。若反应前向D中加入几滴酚酞,溶液呈红色,产生此现象的原因是 ;反应结束后D中的现象是 。
乙酸乙酯是无色具有水果香味的液体,沸点为77.2 ℃,实验室某次制取它用冰醋酸14.3 mL、95%乙醇 23 mL。还用到浓硫酸、饱和碳酸钠以及极易与乙醇结合成六水合物的氯化钙溶液。主要装置如图所示: 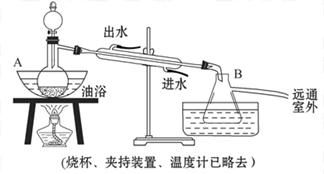
实验步骤:
①先向A中的蒸馏烧瓶中注入少量乙醇和浓硫酸后摇匀,再将剩下的所有乙醇和冰醋酸注入分液漏斗里待用。这时分液漏斗里冰醋酸和乙醇的物质的量之比约为5∶7。
②加热油浴保温约135 ℃~145℃
③将分液漏斗中的液体缓缓滴入蒸馏烧瓶里,调节加入速率使蒸出酯的速率与进料速率大体相等,直到加料完成。
④保持油浴温度一段时间,至不再有液体馏出后,停止加热。
⑤取下B中的锥形瓶,将一定量饱和Na2CO3溶液分批少量多次地加到馏出液里,边加边振荡,至无气泡产生为止。
⑥将⑤的液体混合物分液,弃去水层。
⑦将饱和CaCl2溶液(适量)加入到分液漏斗中,振荡一段时间后静置,放出水层(废液)。
⑧分液漏斗里得到的是初步提纯的乙酸乙酯粗品。
试回答:
(1)实验中浓硫酸的主要作用是_________________。
(2)用过量乙醇的主要目的是_________________。
(3)用饱和Na2CO3溶液洗涤粗酯的目的是___________。
如果用NaOH溶液代替Na2CO3溶液将引起的后果___________________________________。
(4)用饱和CaCl2溶液洗涤粗酯的目的是___________。
(5)在步骤⑧所得的粗酯里还含有的杂质是_________。
某研究性学习小组设计了一组实验验证元素周期律。
(1)甲同学在a、b、c三只烧杯里分别加入50 mL水,再分别滴加几滴酚酞溶液,依次加入大小相近的锂、钠、钾块,观察现象。
①甲同学设计实验的目的是________________________________________________;
②反应最剧烈的烧杯是_______(填字母);
③写出b烧杯里发生反应的离子方程式_____________。
(2)乙同学设计实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强。他设计了下图装置以验证碳、氮、硅元素的非金属性强弱。
乙同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到白色沉淀生成。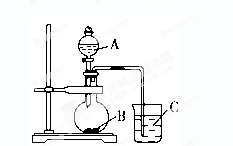
①写出所选用物质的化学式:A、________; B、________;C、________。
②写出烧瓶中发生反应的化学方程式:
___________________________________________________________。
③写出烧杯中发生反应的化学方程式:
___________________________________________________________。
④碳、氮、硅元素的非金属性强弱顺序为_______________________。
已知在同温时氨水的电离平衡常数与醋酸的电离平衡常数相等,溶有一定量的氯化铵溶液呈酸性。现向少量的Mg(OH)2悬浊液中加入适量的饱和氯化铵溶液,固体完全溶解,对此:
甲同学的解释是:Mg(OH)2(s) Mg2++2OH-①
Mg2++2OH-①
NH4++H2O NH3·H2O+H+②
NH3·H2O+H+②
H++OH-=H2O③
由于NH4+水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解。
乙同学的解释是: Mg(OH)2(s) Mg2++2OH-①
Mg2++2OH-①
NH4++OH- NH3·H2O②
NH3·H2O②
由于NH4Cl电离出的NH4+与Mg(OH)2电离出的OH-结合,生成了弱电解质NH3·H2O,导致反应①平衡右移,沉淀溶解。
(1)丙同学不能肯定那位同学的解释合理,于是,选用下列的一种试剂证明甲、乙两位同学的解释只有一种正确,他选用的试剂是 (填写编号)
| A.NH4NO3 | B.CH3COONH4 | C.Na2CO3 | D.NH3·H2O |
(2)丙同学将所选试剂滴入Mg(OH)2的悬浊液中,Mg(OH)2溶解,由此推知:(填“甲”和“乙”)同学的解释更合理,理由是;
(3)写出NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式。
下面的框图是测定CuSO4·xH2O中结晶水含量的实验流程。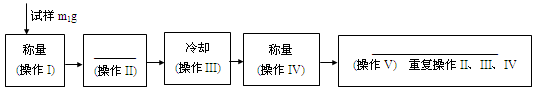
40. 填写流程中空白的操作名称:(操作II)_____________; (操作V)___________________。
41. 其加热装置正确的是____________(填写编号)。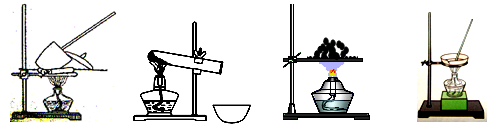
a bcd
42. 重复操作II、III、IV,直到连续两次称量结果相差不超过______g。
43. 操作III必须要在_______(填仪器名称)中进行。
44. 以下胆矾结晶水含量的测定操作正确的是____________(填写编号)。
a. 加热时,晶体溅出坩埚,再加些胆矾
b. 加热时,先用小火,后用大火加热至最后
c. 加热时,不断用玻璃棒搅拌
45. 若实验测得的硫酸铜晶体中结晶水含量偏高,可能的原因有__________(填写编号,下同);若实验测得的硫酸铜晶体中结晶水含量偏低,可能的原因有____________。
a.晶体未完全变白就停止加热
b.加热过程中有少量晶体溅出
c.加热后在空气中自然冷却
海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: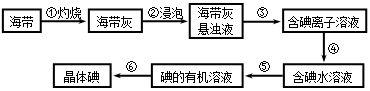
37. 步骤③的实验操作名称是_____________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是_____________。
38. 步骤④需加入的试剂是________,反应的离子方程式是____________________。
39. 步骤⑤中,某学生选择用苯来提取碘,理由是_______________________________,
_________________________________________。