下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。请回答下列问题:
(1)当电极a为Al、电极b为Cu、电解质溶液为稀硫酸时,写出该原电池的总的离子反应反应方程式:
正极的电极反应式为:
当a极溶解的质量为5.4g时,有 mol电子通过导线
(2)当电极a为Al、电极b为Mg、电解质溶液为氢氧化钠溶液时,
该装置 (填“能”或“不能”)形成原电池,
若不能,请说明理由 (若能该空不作答),
若能,该原电池的正极为 ;该原电池总的化学反应方程式为:
有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C单质燃烧时呈现黄色火焰,C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)C离子结构示意图:。
(2)AB2的结构式为。
(3)C2D的电子式:。
(4)写出由B、C、D三种元素组成的两种化合物的化学式,。
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴的工艺流程如下图: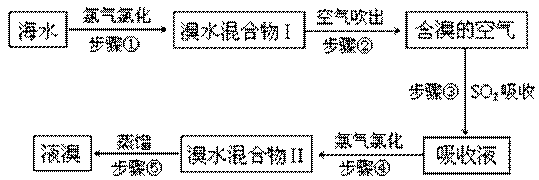
(1)步骤①反应的离子方程式是。
(2)步骤③反应的化学方程式是。
(3)Br的原子序数是,在周期表中位于周期族。
(4)步骤⑤蒸馏的过程中,温度应控制在80~90℃。温度过高或过低都不利于生产,请解释原因:
(5)为什么不直接用“溴水混合物I”而要用“溴水混合物II”进行蒸馏,得到液溴?
A是生产某新型工程塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图所示(图中球与球之间连线代表化学键单键或双键)。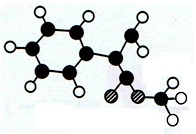
(1)根据分子结构模型写出A的结构简式______________________________。
(2)A在酸性条件下水解生成有机物B和甲醇,与B互为同分异构体的C:含苯环,能发生银镜反应,且苯环上只有一个支链。则C的结构简式为(写二种)_______________、_______________。
(3)拟以芳香烃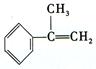 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下: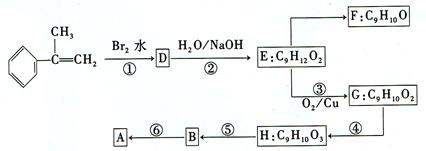
①写出反应类型:反应①属_______________反应,反应④属_______________反应,反应⑤属_______________反应。
②写出结构简式:D_______________,H_______________。
③已知在F分子中含“CH3OH”,通过F不能有效地、顺利地获得B,其原因是___________________________________________。
④写出反应方程式(注明必要的反应条件):
D→E:____________________________________________________________;
B→A:____________________________________________________________。
有常见A、B、C三种短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个;甲、乙、丙是三种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7,丁为气体,戊为淡黄色固体,甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图: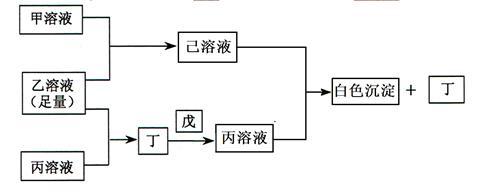
请回答:
(1)写出C元素的原子结构示意图__________________________。
写出丁和戊的电子式:__________________________。
(2)用有关化学用语解释乙溶液呈酸性的原因:__________________________。
丙溶液呈碱性的原因:_______________________________________。
(3)写出有关反应的离子方程式:_____________________________。
①乙溶液+丙溶液→丁:_____________________________________________。
②己溶液+丙溶液→丁:_____________________________________________。
(1)下列实验设计或操作合理的是_________________。
a. 中和热测定实验时,如果没有环形玻璃棒,可用环形铜质搅拌棒代替。
b. 实验室制肥皂时,将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂。
c. 实验室制取乙烯时必须将温度计的水银球插入反应液中,测定反应液的温度。
d. 向Na2CO3与NaOH的混合溶液中加入足量的CaCl2溶液,再滴加几滴酚酞试液,可检验NaOH的存在。
e. 将10滴溴乙烷加入1 mL 10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子。
(2)①取等体积、等物质的量浓度的盐酸和乙酸溶液分别与等量(足量)相同的锌反应,通过生成H2的快慢证明乙酸是弱酸。取用“相同”的锌的目的是_____________________________,比较生成H2快慢的方法是_____________
______________________________________。
②做溴乙烷水解实验时,不断振荡乙烷与NaOH溶液混合物的作用是____________________,溴乙烷已完全水解的现象是___________________。