某化学实验小组,通过Li3N固体水解生成氢氧化锂和氨气的反应制氨气,并进行氨气还原氧化铜的实验探究。如下图所示,给出了本实验可供选择的装置: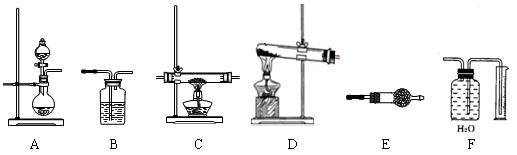
请回答下列问题:
(1)按该方法制氨气时,应选用上述装置中的 (填装置代码,下同)做氨气发生装置。
(2)为检验氨气还原氧化铜反应后生成Cu、H2O、N2,氨气发生装置后应依次连接 → C → → →
(3)在C装置前后连接的装置中,填充的药品按前后顺序分别为 、 。
(4)有资料提出:CuO被还原时,当黑色固体完全变为红时,不一定完全转化为Cu,可能还含有Cu2O。已知查阅到一离子反应方程式:Cu2O+2H+=Cu2++Cu+H2O。依据该信息,若证明C处的红色固体中是否含有Cu2O ,请设计实验: 。
(5)实验时充分加热,至C装置质量不再减轻为止。实验完毕后,若实验测得收集的N2体积为aL(已折算为标准状况)。则若用CH4还原同样多CuO,理论上最少需要CH4的体积为(标准状况,用含字母a的代数式表示) L。
某教师在课堂上用下图所示的装置来验证浓硫酸与铜是否发生反应,并探讨反应所产生气体的性质。请回答下列问题:
①通过试管乙中发生的 现象说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有 性。
②写出试管甲中所发生反应的化学方程式 。
③该反应体现了浓硫酸的性和性。
除去Na2CO3粉末中混入的NaHCO3杂质用 方法,化学方程式为。
对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、分液等。下列各组混合物的分离或提纯应采用什么方法?
①提取碘水中的碘,可用法;
②从氢氧化铜的悬浊液中分离出氢氧化铜,可用法;
③除去食盐水中的水,可用法;
④分离植物油和水,可用法。
某中学化学实验小组为了证明和比较SO2与氯水的漂白性,设计了如下装置:
(1)实验室常用装置E制备Cl2,指出该反应中浓盐酸所表现出的性质是______、_______。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪色,停止通气后,给B、D两个试管加热,两个试管中的现象分别为:B , D_________________。
(3)装置C的作用是________________________________。
(4)该实验小组的甲、乙两位同学利用上述两发生装置按下图装置继续进行实验:
通气一段时间后,甲同学实验过程中品红溶液几乎不褪色,而乙同学的实验现象是品红溶液随时间的推移变得越来越浅。试根据该实验装置和两名同学的实验结果回答问题。
①试分析甲同学实验过程中,品红溶液不褪色的原因是:
。
②你认为乙同学是怎样做到让品红溶液变得越来越浅的?
(6分)右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。
Ⅰ.硫酸具有A-D所示的性质,以下过程主要表现了浓硫酸的那些性质?请将选项字母填在下列各小题的括号内:
A强酸性 B 吸水性 C 脱水性 D 强氧化性
(1)浓硫酸可以干燥氢气()
(2)浓硫酸使木条变黑()
(3)热的浓硫酸与铜片反应()
Ⅱ.现用该浓硫酸配制100 mL 1 mol/L的稀硫酸。可供选用的仪器有: ①胶头滴管; ②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平;⑦玻璃棒; ⑧100mL容量瓶。请回答:
(1)配制稀硫酸时,上述仪器中不需要使用的有(选填序号)。
(2)经计算,配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为 mL。
(3)下列操作会使配制的溶液浓度偏高的是()
| A.量取浓H2SO4时,俯视刻度线 | B.定容时,俯视容量瓶刻度线 |
| C.配制前,容量瓶中有水珠 | D.定容后摇匀发现液面下降而未向其中再加水 |