A、B、C是三种短周期元素,其中A元素原子M层上电子数比L层少2个电子;B元素原子比A元素原子的电子层少,又知B元素最高正价与负化合价的绝对值相等;C 元素的阳离子核外电子排布与Ne原子核外电子排布相同;且又知这三种元素可组成BA2型共价化合物和C2A型离子化合物。由上述条件回答下列问题:
(1)A、B、C三元素的名称分别是:A_______,B_______,C_______。
(2)化合物C2A的电子式是______________。
(3)化合物BA2的化学式是______________。
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
①2SO2(g)+O2(g) 2SO3(g)的△H0(填“>”或“<”);若在恒温、恒
2SO3(g)的△H0(填“>”或“<”);若在恒温、恒
压条件下向上述平衡体系中通入氦气,平衡移动(填“向左”、“向右”或“不”);
若在固定容积的密闭容器中发生反应,起始时SO2和O2分别为1mol和0.5mol,达到平衡时SO2的转化率为90%。则从SO3开始进行反应,在相同条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量,转化率为
②若温度为T1、T2,反应的平衡常数分别为K1、K2,则K1K2;若反应进行到状
态D时,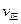
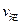 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(2)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
①写出自然界固氮的化学反应方程式:。
②氨气溶于水得到氨水。在25°C下,将a mol·L-1的氨水与b mol·L-1的盐酸等体积混合,反应后溶液中显中性,则c(NH4+)c(Cl-)(填“>”、“<”或“=”);用含a和b的代数式表示出氨水的电离平衡常数表达式。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合态存在。在25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入适量的0.1mol·L-1硝酸银溶液,有白色沉淀生成。向反应后的浊液中,继续加入0.1mol·L-1的NaI溶液,看到的现象是,产生该现象的原因是(用离子方程式表示)。
(已知25°C时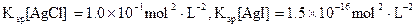 )
)
已知:相同温度时,一元弱酸HA的Ka比一元弱酸HB的Ka大。试比较相同温度相同体积的下列两溶液中离子数目的多少。(填“=”、“ >”、“<”、“无法确定”)
(1)物质的量浓度相等的NaA溶液(n1)与NaB溶液(n2),n1n2
(2)pH相等的NaA溶液(n1)与NaB溶液(n2),n1 n2
n2
(3)c(A—)与c(B—)相等的NaA溶液(n1)与NaB溶液(n2),n1n2
已知某温度下,Kw=l×10-13。A为酸溶液,其pH=a;B为碱溶液,其pH=b。
(1)若A为强酸,B为强碱,且a + b=13,两者等体积混合后,溶液的pH=;若此时溶液中阳离子浓度大于阴离子浓度,其原因可能是(用文字表述)___________________________________________________________
(2)若A的化学式为HR, B的化学式为MOH,且a + b = 13。若两者等体积混合
后溶液显碱性,则其原因可能是_________________________________________,
此混合后的溶液中,微粒浓度大小关系一定正确的是_______________填序号)。
① c(MOH)> c ( M + ) > c ( R一)> c ( H + ) > c ( OH一)
② c ( HR ) > c ( M + ) > c ( R一)> c ( OH一)> c ( H + )
③ c(M +)> c ( R一)> c ( H + ) > c ( OH一)
④ c ( M + ) > c ( R一)> c ( OH一)>c(H +)
⑤ c ( M + ) + c ( H + ) =" c" ( R 一)+ c ( OH一)
⑥ c ( MOH ) =" c" (H +)-c(OH一)
在0.5L的密闭容器中,一定量的氮气和氢气进行
如下化学反应:N2(g)+3H2(g) 2NH3(g) ⊿H<0,其化学平衡常数K与温度t的关系如右表:
2NH3(g) ⊿H<0,其化学平衡常数K与温度t的关系如右表:
| t/℃ |
200 |
300 |
400 |
| K |
K1 |
K2 |
0.5 |
请完成下列问题;
(1)试比较K1、K2的大小,K1K2(填写“>”、“=”或“<”)
(2)下列各项能作为判断该反应达到化学平衡状态 的依据是(填序号字母)
的依据是(填序号字母)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.υ(N2)正=3υ(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
(3)400℃时,反应2NH3(g)  N2(g)+3H2(g)的化学平衡常数的值为。
N2(g)+3H2(g)的化学平衡常数的值为。
当测得NH3和N2、H2的物质的量分别为3 mol和2 mol、1 mol时,则该反应的
υ(N2)正υ(N2)逆(填写“>”、“=”或“<”)
(4)(3)中反应平衡时,升高温度,NH3转化率(填“变大”、“变小”、“不变”)
有以下几种物质①干燥的食盐晶体②液态氯化氢③水银④蔗糖⑤冰醋酸(纯醋酸晶体)⑥KNO3溶液⑦CaCO3固体⑧SO3填空回答(填序号):
(1)以上物质能导电的是;(2)以上物质中属于非电解质的是;(3)以上物质中属于电解质的是;(4)属于强电解质的是。