在下列物质中选择相应的序号填空:
①甲烷②乙烯③溴乙烷④甲苯⑤1-丁醇⑥乙酸乙酯⑦苯酚⑧乙二酸
(1)分子结构为正四面体的是 ;
(2)能与碳酸氢钠溶液反应的是 ;
(3)能发生水解反应的是 ;
(4)能与溴水反应并使其褪色但无白色沉淀生成的是  ;
;
(5)能使FeCl3溶液变紫色的是 ;
(6)能发生消去反应的是 。
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的处理。
(1)为检测PAFC中铝和铁元素的含量,采用如图所示流程进行。
回答下列问题:
①PAFC中铁元素的化合价为_________。
②步骤I中的试剂A是(从“氢氧化钠溶液”、“氨水”中选择)
步骤Ⅲ中的试剂B是。
③步骤Ⅱ的操作是,用到的主要玻璃仪器。
(2)某工厂欲以工业废料(铁、铁和铝的氧化物)为原料制取PAFC,设计如下流程:
①在废料中加入过量稀盐酸,发生多个离子反应,请在空白处补全离子方程式:
FeO+2H+ Fe2++H2O Al2O3+6H+
Fe2++H2O Al2O3+6H+ 2Al3++3H2O
2Al3++3H2O
Fe2O3+6H+ 2Fe3++3H2O
2Fe3++3H2O
②所得酸性溶液中,不能确定是否一定存在的阳离子是(填序号)。
A.Al3+ B.Fe2+ C.Fe3+ D.H+
为证明该离子确实存在,可采用的操作(必须指明所采用的试剂及观察到的现象)是:。
③往酸性溶液中加入试剂X的目的是(用离子方程式表示)。
某同学设计如下实验方案,分离KCl和BaCl2两种固体混合物。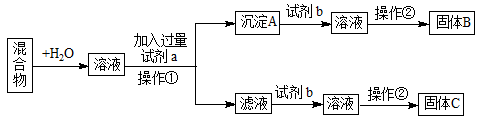
试回答下列问题:
(1)试剂a是;试剂b是;固体B是。(填化学式)
(2)操作②的名称是:、、干燥。
(3)加入试剂a所发生的离子方程式为:。
沉淀A与试剂b所发生的离子方程式为:。
已知钙的金属活泼性介于钾和钠之间,其化学性质与钠相似。钙及其化合物的有关反应如下:
①Ca+2H2O Ca(OH)2+H2↑②CaO+H2O
Ca(OH)2+H2↑②CaO+H2O Ca(OH)2
Ca(OH)2
③CaO2+H2O ④CaO+CO2
④CaO+CO2 CaCO3
CaCO3
⑤2CaO2+2CO2 2CaCO3+O2
2CaCO3+O2
结合所学知识完成下列问题:
(1)完成上述③的化学方程式: CaO2 + H2O ;
;
(2)用双线桥标出反应①的电子转移方向和数目:Ca+2H2O Ca(OH)2+H2↑
Ca(OH)2+H2↑
(3)写出以钙为原料制取过氧化钙(CaO2)的化学方程式:;
(4)在CaO2的水溶液中,滴入酚酞溶液,预期的实验现象可能是;在该溶液中加入少量的MnO2固体,有气泡生成,写出该反应的化学方程式。
Ⅰ.根据条件回答下列问题:
下图是医院病人输液使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液标签,请认真观察标签所列内容后填写:
(1)该葡萄糖注射液属于分散系中的(从“溶液”、“胶体”、“浊液”中选择)。
(2)葡萄糖的摩尔质量为。
(3)已知该葡萄糖注射液的密度是1g/mL,其物质的量浓度为(列式计算)。
Ⅱ.钠与水反应的过程如下图所示。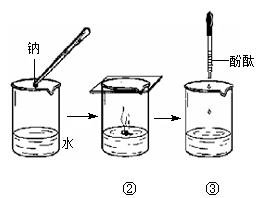
请回答:
(1)钠与水反应的化学方程式为;
(2)根据②中的实验现象,说明钠的密度比水的(填“大”或“小”)。
(3)③中滴入酚酞试液后,可观察到溶液变色。
(4)在实验室中通常将钠保存在里。
一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol·L-1的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.10mol。
(1)上述变化中涉及三个化学反应,其中一个反应为H2 +Cl2 2HCl,请写出另外两个反应的离子方程式:、。
2HCl,请写出另外两个反应的离子方程式:、。
(2)参加反应的氢气和氯气的物质的量之比n(H2) : n(Cl2)为。
(3)工业制取漂白粉的原料是氯气和石灰乳,漂白粉的有效成分为。