硫化钠和碳酸钠为原料、采用下述装置制备硫代硫酸钠,制备反应可表示为:
2Na2 S +Na2CO3 + 4SO2  3Na2S2O3 +CO2。根据要求回答问题:
3Na2S2O3 +CO2。根据要求回答问题: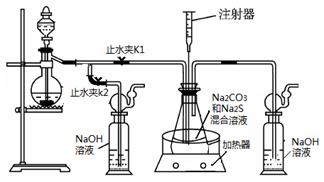
(1)实验时,打开K1,关闭K2,最后洗气瓶中发生反应的离子方程式是 。
(2)锥形瓶内溶液pH小于7时会导致产品分解,因此实验过程中需要控制锥形瓶内溶液的pH。
①反应过程中,锥形瓶中溶液pH将________(填“增大”、“减小”或“保持不变”)。
②测量锥形瓶中溶液pH时,用注射器吸取溶液样品比直接打开锥形瓶中瓶塞取样,除操作简便外,还具有的优点是 。
③若实验过程中测得溶液pH已接近于7。此时应该进行的操作是 。
(3)已知:2Na2 S2O3 +I2="2NaI+" Na2 S4O6。实验结束后进行相关处理,可即获得Na2 S2O3 ·5H2O晶体。为测量其纯度,取晶体样品mg,加水溶解后,滴入几滴淀粉溶液,用0.010mol/L碘水滴定到终点时,消耗碘水溶液vmL,则该样品纯度是 。
(4)制取硫代硫酸钠的另一种方法是直接将硫粉和亚硫酸钠、水混合共热制取。为探究制取硫代硫酸钠最佳条件(溶液pH、亚硫酸钠浓度、反应温度、硫粉质量),设计如下对比实验(每次实验时亚硫酸钠质量均为63g,反应时间为30min):
| 实验序号 |
溶液pH |
亚硫酸钠与水的质量比 |
反应温度 |
硫粉质量 |
亚硫酸钠转化率 |
| 1 |
10 |
1.5:1 |
100 |
18 |
80.7% |
| 2 |
a |
1.1:1 |
100 |
18 |
94.6% |
①实验1、2的目的是探究亚硫酸钠浓度对亚硫酸钠转化率的影响,则a=
②若还要探究溶液pH、反应温度、硫粉质量对亚硫酸钠转化率的影响,除实验1、2外,至少还需进行 次对比实验
③实验表明:亚硫酸钠转化率不受硫粉质量多少的影响。为什么?
答:________________________________________ ___。
下图为实验室干馏煤的装置图,请回答下列问题: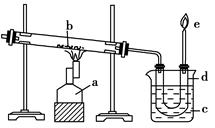
(1)指出图中各仪器的名称:a________;b:________;c:________;d:________。
(2)装置c的作用是________,d中的液体有________和________。其中的无机物里溶有________,可用________检验出来;有机化合物可以通过________的方法使其中的重要成分分离出来。在170~230 ℃时可得到________,加热到230 ℃以上可以得到________。
(3)e处点燃的气体主要是________,火焰的颜色是________色。
实验室用NaOH固体配制200mL 1.25mol/L的NaOH溶液,填空并请回答下列问题:
(1)配制200mL 1.25mol/L的NaOH溶液
| 应称取NaOH的质量/g |
应选用容量瓶的规格/mL |
除容量瓶外还需要的其它玻璃仪器 |
(2)容量瓶上需标有以下五项中的;A
①温度②浓度③容量④压强⑤刻度线
(3)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次);
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)操作A中,将洗涤液都移入容量瓶,其目的是,溶液注入容量瓶前需恢复到室温,这是因为_____________________________;
(5)下列配制的溶液浓度偏低的是;
A、称量NaOH时,砝码错放在左盘
B、向容量瓶中转移溶液时不慎有液滴洒在容量瓶外面
C、加蒸馏水时不慎超过了刻度线
D、定容时俯视刻度线
E、配制前,容量瓶中有少量蒸馏水
(5分)对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、加热分解等。下列各组混和物的分离或提纯应采用什么方法?
(1)实验室中的石灰水久置,液面上常悬浮有CaCO3微粒。可用的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒。
(2)提取碘水中的碘,用方法。
(3)除去食盐溶液中的水,可采用的方法。
(4)淡化海水,可采用的方法。
(5)除去氧化钙中的碳酸钙可用的方法
常温下,取两片质量相等、外形和组成相同表面经过砂纸打磨(完全除掉了氧化物)的铝片,分别加入到盛有体积相同、c(H+)相同的稀硫酸和稀盐酸溶液的两支试管(相同体积)中制取H2。实验现象如下表:
| 时间 酸 |
1 min |
2 min |
5 min |
15 min |
20 min |
| 3mol/L HCl |
少量气泡 |
较多气泡 |
大量气泡 |
反应剧烈 |
铝片耗尽 |
| 1.5mol/L H2SO4 |
均无明显现象(无气泡) |
(1)写出以上反应的离子方程式______________________________________。
(2)分析上表数据,你得出的结论是:。
(3)你认为出现以上现象的可能原因是(写出一个即可):
______________________________________________________;
(4)请设计实验对你的假设进行验证:
__________________________________________________________;
(5)如果上述假设都成立,要使以上稀硫酸与铝反应产生的氢气速率加快,可以采取的措施有(列举三个):
盐酸或硫酸和氢氧化钠溶液的中和反应没有明显的现象。某学习兴趣小组的同学为了证明氢氧化钠溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案。请回答有关问题。
(1)方案一:如图1装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上。开始时使右端U形管两端红墨水相平。实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内氢氧化钠溶液混合,此时观察到的现象是_________,原因是___________。
(2)方案二:该小组借助反应溶液温度的变化来判断反应的发生。如果氢氧化钠溶液与盐酸混合前后有温度的变化,则证明发生了化学反应。该小组同学将不同浓度的氢氧化钠溶液和盐酸各10 mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表:
| 编号 |
盐酸 |
氢氧化钠 |
△t/℃ |
| 1 |
0.1 mol·L-1 |
0.05 mol·L-1 |
3.5 |
| 2 |
0.1 mol·L-1 |
0.1 mol·L-1 |
x |
| 3 |
0.2 mol·L-1 |
0.2 mol·L-1 |
14 |
则x=____________。
(3)方案三:该小组还设计了如图2示装置来证明氢氧化钠溶液确实与稀硫酸发生了反应。他们认为若洗气瓶中导管口有气泡冒出,则说明该反应放出热量,从而证明发生了反应。
①实验时,打开分液漏斗活塞,发现导管流出液体不畅,原因可能是______________
②从原理上讲,该实验设计的不合理之处为__________________________________。
请你在此实验装置的基础上提出修改方案__________________________________。