已知碱金属的氧化物有:普通氧化物,如Li2O;过氧化物,如Na2O2;超氧化物,如KO2;臭氧化物,如RbO3,其中后三者均能与H2O或CO2反应产生O2。
(1)宇航工业,为了能保持飞船座舱内空气成分的稳定,宇航科学家进行了大量的探索,有的科学家提出了“金属过氧化物处理系统”。即不断把座舱内的空气通过盛有金属过氧化物(以过氧化钠为例)的容器,并把处理后的气体充入座舱。每个宇航员平均每天需要消耗0.9 kg氧气,呼出1.0 kg二氧化碳。有关反应的化学方程式为 、 ;将处理后的气体充入座舱时,为了能保持飞船座舱内空气成分的稳定,还应采取的措施是___________________________________。
(2)人体内O2—离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式: O2— + H2O = H2O2+ O2+
(3)Na2O2、K2O2、CaO2以及Ba O2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是 (写电子式)
O2都可与酸作用生成过氧化氢,目前实验室制取过氧化氢可通过上述某种过氧化物与适量稀硫酸作用,过滤即可制得。最适合的过氧化物是 (写电子式)
(4)高温下,超氧化钾晶体 呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则每个超氧化钾晶胞含有 个K+和 个O2-;该晶体中,0价氧原子与-2价氧原子的数目比为
呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则每个超氧化钾晶胞含有 个K+和 个O2-;该晶体中,0价氧原子与-2价氧原子的数目比为 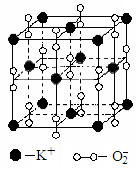
483 g Na2SO4·10H2O中所含的Na+的物质的量是mol,SO42—的物质的量是mol,所含H2O分子的数目是个。
现有K 、O、S、H四种元素,选用其中一种或几种元素可组成符合下列要求的物质(酸、酸性氧化物、盐、X)。
(1)完成下列转化:(用化学方程式表示)
①酸 →盐: ;
;
②酸性氧化物 → 盐:;
(2)X在水溶液中电离成K+ 、H+、SO42-,则X的化学式为,X属于(填序号)
| A.酸 | B.碱 | C.盐 | D.氧化物 |
(3)设计两种实验方案(指出使用的试剂或方法) 鉴别Na2SO4和X:
鉴别Na2SO4和X:
方案1:。
方案2:。
(8分)有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行如下实验:
①取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液。
②继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生。
③取少量②中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶。
根据上述实验现象判断:
⑴该白色固体中一定含有,一定不含有,可能含有。(填化学式)
⑵若要检验未确定的物质是否存在,请说明如何操作(含现象和结论): 。
。
在生活中根据不同的分类标准可以将分散系分为各种类型,例如根据分散质不同可将分散系分为溶液、胶体和浊液,其中分散质微粒的直径在之间的分散系叫做胶体,胶体有很强的吸附能力,在日常生活中通常作为剂。
(1)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO)∶CO(g)+2H2(g) CH3OH(g).
CH3OH(g).
根据题意和所给图象完成下列各题:
①反应达到平衡时,平衡常数表达 式K=,
式K=,
②升高 温度,K值(填“增大”“减小”或“不变”)
温度,K值(填“增大”“减小”或“不变”)
(2)一定温度下,将3 mol A气体和1 mol B气体通入一密闭容器中,发生如下反应:3A(g) + B(g)  xC(g) 请填写下列空白:若容器体积固定为2 L,反应2 min时测得剩余0.6 mol B,C的浓度为0.4 mol/L。
xC(g) 请填写下列空白:若容器体积固定为2 L,反应2 min时测得剩余0.6 mol B,C的浓度为0.4 mol/L。
①x=
②若反应经4 min达到平衡,平衡时C的浓度________ 0.8 mol/L(填“大于”、“等于”或“小于”)。
③平衡混合物中,C的体积分数为22%,则B的转化率是______________。
(3)运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义。
①合成氨反应N2 (g)+3H2(g) 2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡移
2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,则平衡移 动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。
动(填“向左”“向右”或“不”);使用催化剂,上述反应的△H________(填“增大” “减小” 或“不改变”)。
②有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl—NH4Cl为电解质溶液制造新型燃烧电池,放电过程中,溶液中铵根离子浓度逐渐增大。请写出该电池的正极反应式 。
。