某元素原子的质量数为A ,它的离子Xn+核外有y个电子,Wg这
,它的离子Xn+核外有y个电子,Wg这 种元素的原子核内中子数为
种元素的原子核内中子数为
A.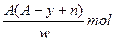 |
B.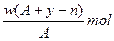 |
C.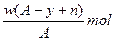  |
D.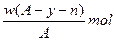 |
下列说法正确的是
①pH=2和pH=1的H2SO4中c(H+)之比为1∶10
②0.2mol·L-1与0.1mol·L-1醋酸中,c(H+)之比大于2∶1
③纯水在80℃和20℃时,pH相等
④FeCl3溶液中c(Fe3+)与c(Cl-)之比为1∶3
⑤同温时,pH=10的Ba(OH)2溶液和pH=10的KCN溶液中由水电离的OH-浓度后者大
⑥100mL 0.1 mol·L-1的醋酸与10 mL 1.0 mol·L-1的醋酸中H+的数目,前者多
| A.①④⑤ | B.①⑤⑥ |
| C.①②⑤ | D.①②③⑥ |
用标准盐酸滴定未知浓度的NaOH溶液时,若测定结果偏高,则产生误差的原因可能是
| A.滴定时,装NaOH溶液的锥形瓶未用NaOH溶液润洗 |
| B.酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D.滴定前仰视读取了酸式滴定管的读数,滴定后读数正确 |
水的电离平衡曲线如图所示,下列说法不正确的是
| A.图中四点Kw间的关系:A=D<C<B |
| B.若从A点到C点,可采用:温度不变在水中加入少量NaAc固体 |
| C.若从A点到D点,可采用:温度不变在水中加入少量酸 |
| D.若处在B点所在的温度,将pH=2的硫酸与pH=10的NaOH的两种溶液等体积混合后,溶液显中性 |
在下列各组反应中,两者反应遵循的化学原理相同的是
| A.KClO3+6HClKCl+3Cl2↑+3H2O和2Na2S+3H2SO3===2Na2SO3+3S↓+3H2O |
| B.稀硫酸溶解FeO和稀硝酸溶解FeO |
| C.过氧化钠的漂白性和SO2水溶液的漂白性 |
| D.泡沫灭火器灭火和干粉灭火器灭火 |
与pH类似,我们定义pOH=-lgc(OH-),下列溶液,一定呈中性的是
| A.c(H+)=1×10-7mol·L-1的溶液 |
| B.水电离的H+和OH-浓度相等的溶液 |
| C.pH+pOH=14的溶液 |
| D.pH=pOH的溶液 |