(14分) 下图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精。已知D在标准状况下的密度为1.25 g/L,其产量可以用来衡量一个国家石油化工发展水平。E是生活中常见的一种有机物。各物质间转化关系如下: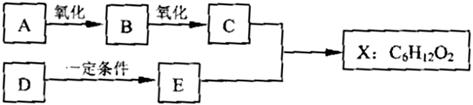
请回答下列问题。
(1)A的名称是 。
(2)B中所含的官能团是 。
(3)C+E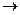 X的化学反应类型是 反应。
X的化学反应类型是 反应。
(4)写出任意两种与A具有相同官能团的A的同分异构体的结构简式(不含A):
、 。
(5)X与氢氧化钠溶液反应的化学方程式是
。
(6)以D为原料生产一种常见塑料的化学方程式是
。
已知:

为合成某种液晶材料的中间体M,有人提出如上不同的合成途径
(1)常温下,下列物质能与A发生反应的有(填序号)
a.苯 b.Br2/CCl4 c.乙酸乙酯 d.KMnO4/H+溶液
(2)M中官能团的名称是,由C→B反应类型为。
(3)由A催化加氢生成M的过程中,可能有中间生成物和(写结构简式)。
(4)检验B中是否含有C可选用的试剂是(任写一种名称)。
(5)物质B也可由C10H13Cl与NaOH水溶液共热生成,写出由C10H13Cl和NaOH水溶液共热反应的化学方程式。
(6)C的一种同分异构体E具有如下特点:
a.分子中含—OCH2CH3 b.苯环上只有两种化学环境不同的氢原子
写出E在一定条件下发生加聚反应的化学方程式。
A、B、C、D、E是中学常见的几种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
回答下列问题:
(1)X的单质与A反应的化学方程式是________________________________。
(2)若C溶液显碱性,则试剂1是 ____溶液(写化学式);若C溶液显酸性,则显酸性的原因是(用离子方程式表示)。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是;
②写出D→E反应的离子方程式;
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠(NaNO2)为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是:。
某课外小组对一些金属单质和化合物的性质进行研究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 |
实验现象 |
| ①将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中。 |
产生气泡,析出疏松的红色固体,溶液逐渐变为无色。 |
| ②反应结束后分离出溶液备用。 |
|
| ③红色固体用蒸馏水洗涤后,置于潮湿空气中。 |
一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3]。 |
按实验中发生反应的现象写出下列化学方程式(是离子反应的只写离子方程式)
①析出疏松的红色固体;
③一段时间后固体由红色变为绿色。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可观察到的现象是。
解释此现象的离子方程式是、。
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来治炼金属锰。
①用铝与软锰矿冶炼锰的原理是(用化学方程式表示)
。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化后的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是。
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图。请针对以下三种不同情况回答: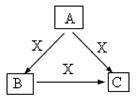
(1)若A、B、C中均含同一种常见金属元素,该元素在 C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素的原子结构示意图为。
②该金属元素的单质与某红色氧化物在高温下反应,可用于焊接铁轨及定向爆破,已知:1mol该单质完全反应,当温度恢复至298K时,共放热QkJ,请写出该反应的热化学反应方程式为。
(2)若A、B、C的焰色反应均呈黄色,水溶液均为碱性。
①用化学方程式表明B溶液呈碱性的原因。
②自然界中存在B、C和H2O按一定比例结晶而成的固体。取一定量该固体溶于水配成100 mL溶液,测得溶液中金属阳离子的浓度为0.5 mol/L。若取相同质量的固体加热至恒重,剩余固体的质量为___________________。
试回答下列问题:
(1)已知24克A和40克B恰好完全反应生成0.8molC和32克D,则C的摩尔质量为。
(2)如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试根据标签上的有关数据回答下列问题:
①该浓盐酸中HCl的物质的量浓度为mol/L。
②若实验室配制450mL2.38 mol/L的稀盐酸,需用该浓盐酸________ mL,如下图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是______________________(填仪器名称)。
在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________2.38mol/L (填“大于”“等于”或“小于”,下同)。