已知:①A+B2+=A2++B,②D+2H2O=D(OH)2 +H2↑,③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B-2e-=B2+。则A2+、B2+、D2+、E2+的氧化性强弱关系是
| A.D2+﹥A2+﹥B2+﹥E2+ | B.E2+﹥B2+﹥A2+﹥D2+ |
| C.D2+﹥E2+﹥A2+﹥B2+ | D.A2+﹥B2+﹥D2+﹥E2+ |
具有下列电子排布式的原子中,半径最大的是
| A.ls22s22p63s23p5 | B.1s22s22p3 |
| C.1s22s22p2 | D.1s22s22p63s23p2 |
下列物质的熔点高低顺序,正确的是
| A.金刚石>晶体硅>碳化硅 | B.K>Na |
| C.NaF<NaCl<NaBr | D.CI4>CBr4 |
下列晶体熔化时不需要破坏化学键的是
| A.晶体硅 | B.食盐 | C.干冰 | D.金属钾 |
下列分子中,属于含有极性键的非极性分子
| A.CO2 | B.Cl2; | C.NH3; | D.H2O |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
A.CO2的电子式: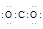 |
B.Cl-的结构示意图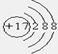 |
| C.乙烯的结构简式 C2H4 | D.质量数为37的氯原子17 37Cl |