硼酸晶体成片状,有滑腻感,可作润滑剂,硼酸分子结构可表示为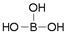 。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐等方面
(1)根据以上所述可知硼酸应属于_____________。
A.强酸 B.中强酸 C.弱酸
(2)研究表明:在大多数情况下, 元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。
元素的原子在形成分子或离子时,其最外电子层具有达到8电子稳定结构的趋势。在硼酸分子中,最外层达到8个电子稳定结构的原子有_______个。
(3)硼酸和甲醇在浓硫酸存在的条件下,可生成挥发性硼酸三甲酯,试写出硼酸完全酯化的化学方程式(注明反应条件)_______________________________________。
(4)已知硼酸0.01mol可被20mL0.5mol·L-1NaOH溶液恰好完全中和,据此推测:硼酸在水中显酸性的原因是(写电离方程式)_________________________________。
碳、氢、氧3种元素组成的有机物A,相对分子质量为152,其分子中C、H原子个数比为1∶1,含氧元素的质量分数为31.58%.A遇FeCl3溶液显紫色,其苯环上的一氯取代物有两种,请回答下列问题:(1)A的分子式是____________________.
(2)若A能与NaHCO3溶液反应,A的结构简式为____________________;写出A与NaHCO3溶液反应的化学方程式__________________________________________________________.
(3)如A可以发生如图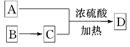 所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式为______________________________________________________。
所示转化关系,D的分子式为C10H12O3,A与C反应的化学方程式为______________________________________________________。
(4)甲、乙两装置均可用作实验室由C制取B的装置,乙图采用甘油浴加热(甘油沸点290℃,熔点18.17℃),当甘油温度达到反应温度时,将盛有C和浓硫酸混合液的烧瓶放入甘油中,很快达到反应温度.甲、乙两装置相比较,乙装置有哪些优点________________________.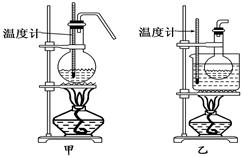
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢原子。
(1)A的结构简式为;
(2)已知A、B、C有下列转化关系,则反应②的化学方程式为;
C的化学名称为。 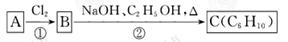
写出下列反应的离子方程式,或相应的化学方程式(每题2分7小题共14分)
(1)石灰石溶于稀盐酸。
(2)稀硫酸与氢氧化钡溶液的反应。
(3)碳酸氢钠溶液与盐酸反应。
(4)氢氧化铜与稀硫酸反应。
(5)2H++ CO32-=CO2↑+H2O 。
(6)Cu+2Ag+=Cu2++2Ag。
(7)CO2+2OH-=CO32-+H2O。
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此回答下列问题:
(1)该硫酸的物质的量浓度为mol/L。
(2)配制250mL 0.92mol·L-1的稀硫酸需取该硫酸mL。
(3)配制时必需的玻璃仪器有:______________________________________________________。
(4)定容时,待容量瓶中溶液的凹液面正好与刻度线相切,盖好瓶塞后的下一步操作是______。
(5)定容时,若加入的水超过刻度线,必须采取的措施是。
(6)下列操作对H2SO4的物质的量浓度有什么影响(偏高、偏低或无影响)?
①转移溶液后,未洗涤烧杯:;
②容量瓶用水洗净后未烘干:;
③定容时俯视容量瓶的刻度线:。
(1)在3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O反应中,_______是氧化剂;_______是还原剂;_______元素被氧化;_______元素被还原;______是氧化产物;_______是还原产物,被还原的HNO3与参加反应的HNO3物质的量之比是_____。用双线桥标出该反应电子转移的方向和数目。
(2)双线桥标出反应KClO3+ 6HCl=KCl + 3 Cl2↑ + 3H2O电子转移的方向和数目。