某合金(仅含铜、铁)中铜和铁的物质的量之和为,其中的物质的量分数为 ,将其全部投入50 的硝酸溶液中,加热使其充分反应(假设是唯一的还原产物)。下列说法正确的是
| A. | 若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 |
| B. | 若金属全部溶解,则溶液中一定含有 |
| C. | 若金属全部溶解,且产生336 气体(标准状况),则 |
| D. | 当溶液中金属离子只有 、 时,则 与 的关系为: |
载人空间站的生态系统中,要求分离人呼出的二氧化碳,同时需要提供氧气。某电化学装置利用太阳能转化的电能可以实现上述要求,同时还有燃料一氧化碳生成,该电化学装置中得电子的电极发生的反应是2CO2+4e-+2H2O===2CO+4OH-。下列判断错误的是
| A.上述电化学装置相当于电解池 |
| B.上述装置进行的总反应为2CO2==2CO+O2 |
| C.反应结束后该电化学装置中的电解质溶液pH增大 |
| D.失电子的电极发生的反应是4OH--4e-==2H2O+O2↑ |
下表为部分短周期元素的原子半径及主要化合价。下列说法正确的是
| 元素符号 |
L |
M |
Q |
R |
T |
| 原子半径 |
0.186 |
0.143 |
0.104 |
0.075 |
0.066 |
| 主要化合价 |
+1 |
+3 |
+6、-2 |
+5、-3 |
-2 |
A.气态氢化物的稳定性:R>T
B.工业上电解MCl3溶液制备单质M
C.化合物L2T与QT2所含化学键类型相同
D.L与Q的最高价氧化物的水化物均能与M(OH)3反应
X、Y、Z为中学化学常见物质,其转化关系如图5所示(“→”表示一步转化)。下列组合不正确的是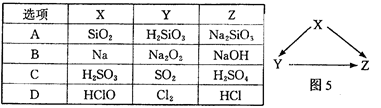
下列表示对应化学反应的离子方程式正确的是
| A.碳酸钙溶于稀醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| B.铜与稀硝酸反应:3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O |
| C.向NH4HCO3溶液中滴加过量Ba(OH)2溶液:HCO3-+OH-+Ba2+=H2O+BaCO3↓ |
D.用银氨溶液检验乙醛中的醛基:CH3CHO+[Ag(NH3)2]++2OH-  CH3COO-+NH4++NH3+ Ag↓+H2O CH3COO-+NH4++NH3+ Ag↓+H2O |
下列有关实验原理、操作或现象不正确的是
| A.图1装置可制得金属锰,用同样的装置可制得金属铬 |
| B.实验室用图2所示装置制取少量氨气 |
| C.实验室用图3所示装置除去Cl2中的少量HCl |
| D.用一束光照射淀粉溶液会产生一条明显的光路 |