下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )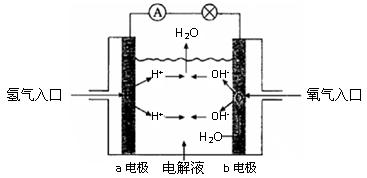
| A.a电极是负极 |
| B.b电极的电极反应式为:4OH--4e-=2H2O +O2↑ |
| C.氢氧燃料电池是一种具有应用前景的绿色电源 |
| D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
萘分子的结构可以表示为  或
或 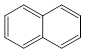 ,两者是等同的。苯并[α]
,两者是等同的。苯并[α]
芘是强致癌物质(存在于烟囱灰、煤焦油、燃烧的烟雾和内燃机的尾气中)。它的分子由5个苯环并
合而成,其结构可以表示为(Ⅰ)或(Ⅱ)式:

(Ⅰ)(Ⅱ)
这两者也是等同的。现有结构A 、B 、 C 、D , 与(Ⅰ)、(Ⅱ)式同分异构体的是 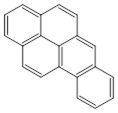

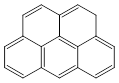

A. B. C. D.
最近科学家公布了新合成的一种烯烃,始祖鸟烯(Pterodactyladiene),形状宛如一只展
翅飞翔的鸟,其键线式如右图,其中R1、R2为烷烃基。则下列有关始祖鸟烯的说法中正确的是 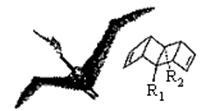
| A.始祖鸟烯与乙烯互为同系物 |
| B.若R1=R2=CH3,则其化学式为C12H16 |
| C.若R1=R2=CH3,则始祖鸟烯的一氯代物有3种 |
| D.始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的 |
在矿井里,必须采取安全措施,如通风、严禁烟火等,而且要随时检查瓦斯的体积分数,
如果空气中含甲烷5%~15%,遇到明火会发生爆炸。发生爆炸最强烈时空气中甲烷所占的体积分数
是
| A.5% | B.9.5% | C.10.5% | D.15% |
科学家致力于CO2的“组合转化”技术研究,把过多的CO2转化为有益于人类的物质,如
将CO2和H2以1∶4的比例混合,通入反应器中,在适当的条件下反应,可获得一种重要的能源,CO2
+4H2→CH4+2H2O若将CO2与H2混合,在一定条件下以1∶3的比例发生反应,生成某种重要的化工
原料和水,该化工原料可能是
| A.烷烃 | B.烯烃 | C.炔烃 | D.芳香烃 |
CH3CH=CHCl有下列反应或现象:①取代反应,②加成反应,③消去反应,④使溴水褪色,⑤使酸性KMnO4溶液褪色,⑥与AgNO3溶液生成白色沉淀,⑦聚合反应。对于该有机物
| A.以上反应均可发生 | B.只有⑦不能发生 |
| C.只有⑥不能发生 | D.只有②不能发生 |