X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是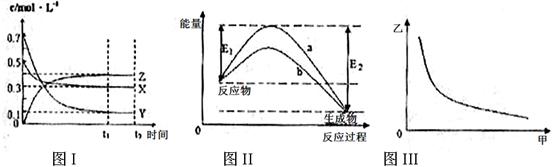
A.该反应热化学方程式为X(g) +3Y(g) 2Z(g)△H= —(E2―E1) 2Z(g)△H= —(E2―E1) |
| B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线 |
| C.若升高温度,该反应的平衡常数减小,Y的转化率降低 |
| D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a一定是没有加入催化剂时的能量变化曲线 |
下列反应中,属于氧化还原反应的是
| A.氢氧化铝受热分解 |
| B.氧化铜与硝酸反应 |
| C.实验室中用高锰酸钾加热分解制取 氧气 |
| D.实验室中用氯化铵固体与氢氧化钙固体制取氨气 |
下列离子方程式中正确的是
| A.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑ |
| B.用小苏打治疗胃酸过多:HCO3- +H+=CO2↑+H2O |
| C.锌片插入硝酸银溶液中:Zn+Ag+= Zn2++Ag |
| D.碳酸氢铵溶液与足量氢氧化钠溶液反应:NH4++OH-=NH3·H2O |
下列各组离子,能在指定溶液中大量共存的是
| A.无色溶液中:Ba2+、HCO3﹣、NO3﹣、K+ |
| B.能使紫色石蕊试剂变红的溶液中:NH4+、NO3﹣、CO32﹣、Na+ |
| C.使酚酞试液变红的溶液:Na+、Ca2+、NO3-、Cl- |
| D.有SO42-存在的溶液中:K+、Ba2+、Ag+、NO3﹣ |
a、b、c、d是HCl、BaCl2、AgNO3、Na2CO3四种溶液中的一种,现将它们两两混合,现象如下表所示:
| 反应物 |
a+b |
c+d |
a+d |
a+c |
b+d |
| 现象 |
白色沉淀 |
白色沉淀 |
白色沉淀 |
白色沉淀 |
无色气体 |
由上述现象可推知a、b、c、d依次是
A.HCl、BaCl2、AgNO3、Na2CO3
B.AgNO3、HCl、BaCl2、Na2CO3
C.BaCl2、Na2CO3、 AgNO3、HCl
D.AgNO3、HCl、Na2CO3、BaCl2
如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离装置是
A. |
B. |
C. |
D.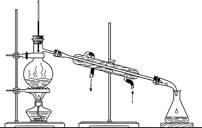 |