下列反应中,能说明碳的非金属性比硅元素强的是( )
A.SiO2+2C Si+2CO↑ Si+2CO↑ |
B.CaCO3+SiO2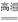 CaSiO3+CO2↑ CaSiO3+CO2↑ |
| C.Na2SiO3+CO2+H20==Na2CO3+H2SiO4↓ |
D.Si+2 NaOH+H2O==Na2SiO3 NaOH+H2O==Na2SiO3 +2H2↑ +2H2↑ |
在一固定容积的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L,0.1 mol/L,0.2 mol/L, 当反应达到平衡时,可能存在的数据是
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2 mol/L,0.1 mol/L,0.2 mol/L, 当反应达到平衡时,可能存在的数据是
| A.SO2为0.4 mol/L,O2为 0.2 mol/L | B.SO2为0.25 mol/L |
| C.SO2、SO3均为0.15 mol/L | D.SO3为0.4 mol/L |
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,放出133.5 kJ热量。则下列热化学方程式中正确的是
| A.N2H4(g)+O2(g)===N2(g)+H2O(g)ΔH=+267 kJ·mol-1 |
| B.N2H4(g)+O2(g)===N2(g)+2H2O(l)ΔH=-133.5 kJ·mol-1 |
| C.N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH=+534 kJ·mol-1 |
| D.N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH=-534 kJ·mol-1 |
某有机物的结构简式为CH2=CH— CH2OH。下列关于该有机物的叙述不正确的是
| A.能与金属钠发生反应并放出氢气 |
| B.能在催化剂作用下与H2发生加成反应 |
| C.在浓H2SO4催化下能与乙酸发生酯化反应 |
| D.能与新制的氢氧化铜悬浊液反应 |
下列化合物既含有共价键又含有离子键的是
| A.H2SO4 | B.Na2O2 | C.MgCl2 | D.C2H5OH |
结合右图判断,下列叙述正确的是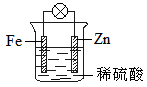
| A.正极被保护 |
| B.H+向Zn电极移动 |
| C.加入少量KSCN溶液,变血红色 |
| D.负极的电极反应式是:Fe-2e-=Fe2+ |