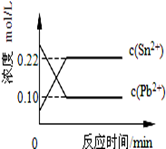
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)⇌Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是( )
| A.往平衡体系中加入金属铅后,C(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
潮湿的氯气、新制的氯水、次氯酸钠、漂白粉溶液均能使有色布条褪色,这是由于它们含有或能生成
| A.氯气 | B.次氯酸 | C.次氯酸根 | D.氯化氢 |
实验室里做钠跟水反应的实验时,用到的仪器和药品是:①试管夹、②镊子、③小刀、④滤纸、⑤研钵、⑥烧杯、⑦坩埚、⑧石棉网、⑨玻璃片、⑩药匙.
| A.①②③④ | B.②③④⑥⑨ | C.③④⑧⑨⑩ | D.②⑤⑦⑨⑩ |
①钠比水轻;②钠的熔点较低;③钠与水反应时要放出热量;④钠与水反应后溶液呈碱性.某学生将一小块金属钠投入滴有酚酞试液的水中,该实验能证明上述四点性质中的
| A.①④ | B.①②④ | C.①③④ | D.①②③④ |
下面是人们对于化学科学的各种常见认识,其中错误的是
| A.化学面对现代日益严重的环境问题显的无能为力 |
| B.化学将在能源、资源的合理开发和安全应用方面大显身手 |
| C.化学是一门具有极强实用性的科学. |
| D.化学是一门以实验为基础的自然科学 |
将23 g钠和24 g镁分别放入等质量的过量的稀硫酸中,得到溶液的质量分别为a g和b g (设反应中水分不损失)则a和b的关系为
| A.a=b | B.a>b | C.a<b | D.无法确定 |