下列离子方程式错误的是( )
| A.硫酸与氯化钡溶液反应: SO42-+ Ba2+ =BaSO4↓ |
| B.碳酸钙与盐酸反应: CaCO3 + 2H+ =Ca2+ + CO2↑ + H2O |
C.钠投入硫酸铜溶液中: 2Na + Cu2+ = 2N a+ + Cu a+ + Cu |
| D.氯气通入水中:Cl2 + H2O = H+ + Cl-+ HClO |
对于某些离子的检验及结论正确的是
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32— |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42— |
| C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
常温下,在100ml 12mol·L—1的浓HNO3中加入足量的铁粉,最终产生标准状况下气体的体积为(不考虑NO2转化为N2O4)
| A.几乎无气体产生 | B.等于6.72L[来 |
| C.等于13.44L | D.介于6.72L至13.44L之间 |
下列反应的离子方程式书写正确的是
| A.硫酸铝溶液中加入过量氨水 Al3++3OH- = Al(OH)3¯ |
B.电解饱和食盐水 2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
| C.钠与水的反应 Na+2H2O = Na++2OH- +H2↑ |
D.单质铜与稀硝酸反应 Cu + 2H++ 2NO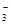 = Cu2+ + 2NO↑+H2O = Cu2+ + 2NO↑+H2O |
下列有关金属的工业制法中,正确的是
| A.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 |
| B.制铁:以铁矿石为原料,CO还原得铁 |
| C.制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁 |
| D.制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如下图所示,由此确定,原溶液中含有的阳离子可能是 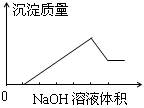
| A.Mg2+、Al3+、Fe3+ | B.Na+、Mg2+、Al3+ |
| C.H+、Ba2+、Al3+ | D.H+、Mg2+、Al3+ |