原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.NaOH + HCl =" NaCl" + H2O,
B.2FeCl3 + Cu = 2FeCl2 + CuCl2
判断能否设计成原电池A. B. 。(填“能”或“不能”)
(2)由铜片、锌片和足量稀H2SO4组成的原电池中,若锌片只发生原电池腐蚀,一段时间后某电极产生3.36L标准状况下的气体。
①负极是 (填“锌”或“铜”),发生 反应(填“氧化”或“还原”);
②正极的电极反应式为 ;
③产生这些气体共需转移电子 mol。
根据下列几种粒子的结构示意图,回答问题:(填粒子符号)
(1)其中属于阴离子的是,
(2)属于金属元素的是,
(3)具有相似化学性质的是。
在化学符号ZAX中,A表示;Z表示。
已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应
① A + H2O → B + C② C + F → D③ D + NaOH 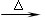 F + E + H2O
F + E + H2O
(1)写出它们的化学式:A、B、 D、
E、F;
(2)写出各步反应的离子方程式,并指反应①的氧化剂和还原剂物质的量比。
①、氧化剂与还原剂物质的量比为:。
②。
③。
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式。
某校高一研究性学习小组将造成我省某市空气污染的主要原因分为以下四种:
| A.燃烧农作物秸秆 | B.燃烧含硫煤 | C.粉尘污染 | D.机动车尾气污染 |
并就造成该市空气污染的最主要原因调查了该市100名市民和100位环保部门人士。调查结果如下图所示: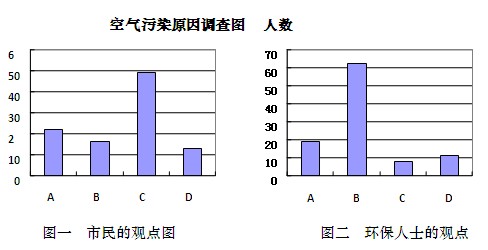
(1)调查结果显示:该市市民认为造成空气污染的最主要原因是,环保人士认为造成该市空气污染的最主要原因是。
(2)调查结果说明市民对造成空气污染的最主要原因认识不足。该最主要原因造成的大气污染的主要有害成分是,空气中该成分含量较高时,在空气中的氧气和水的共同作用下,会形成酸雾,其化学反应方程式为
(3)下列措施能够减少空气中该成分排放量的是
①用天然气代替煤炭做民用燃料②改进燃烧技术,提高热能利用率③工厂生产时将燃煤锅炉的烟囱造得更高④燃煤中加入适量石灰石后使用
用于金属焊接的某种焊条,其药皮由大理石、水泥、硅铁等配制而成。
(1)
的原子结构示意图为;
与
溶液反应的离子方程式为。
(2)
的原子的中子数为;
属于(填离子或共价)化合物。
(3)
与
的电子数相同,
所在族的各元素的氢化物的水溶液均显酸性,则该族氢化物中沸点最低的是。
(4)焊接过程中,药皮在高温下产生了熔渣和使金属不被氧化的气体,该气体是。
(5)经处理后的熔渣36.0
(仅含
、
、
),加入足量稀盐酸,分离得到11.0
固体;滤液中加入过量
溶液,分离得到21.4
固体;则此熔渣中的
质量分数为。