根据废水中所含有害物质的不同,工业上有多种废水的处理方法。
(1)废水I若采用CO2处理,离子方程式是 。
(2)废水II常用明矾处理。实验中发现废水中的c(HCO-3)越大,净水效果越好,这是因为 。
(3)废水III中的汞元素存在如下转化 (在空格上填相应的化学式):
(在空格上填相应的化学式):
Hg2+ =====CH3Hg++H+
我国规定,Hg2+的排放标准不能超过0.05mg/L。某工厂排放的1m3废水中含Hg2+ 3×10-4mol,是否达到了排放标准 (填“是”或“否”)。
(4)废水IV常用Cl2将CN-氧化成两种无毒气体,则该反应的离子方程式为
.
A、B、C、D、E、F都是短周期元素,原子序数依次增大,B、C、D同周期,A、E同主族。A、C能形成两种液态化合物甲和乙,原子个数比分别为2∶1和1∶1。B元素原子有两个未成对电子,D是周期表中电负性最大的元素,F是地壳中含量最多的金属元素。根据以上信息回答下列问题:
⑴ 写出A、C、E三种元素的符号:
A, C, E。
⑵ 甲、乙两分子中含有非极性共价键的是(填分子式),它的电子式为。
⑶ C、D、F的离子中,半径最小的是(填离子符号)
⑷ 在化合物BA4中元素B的杂化方式为:杂化,BA4的空间构型为。
⑸用氢键表示式写出液态D的氢化物中存在的氢键
请回答下面问题
(1)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 |
NaF |
MgF2 |
SiF4 |
| 熔点/K |
1266 |
1534 |
183 |
解释表中氟化物熔点差异的原因:
。
(2)CO的结构可表示为C≡O,N2的结构可表示为N≡N。下表是两者的键能数据:(单位:kJ·mol-1)
| C-O |
C=O |
C≡O |
|
| CO |
357.7 |
798.9 |
1071.9 |
| N-N |
N=N |
N≡N |
|
| N2 |
154.8 |
418.4 |
941.7 |
CO与N2的结构相似,分子中都含有共价三键,其中含有个π键;结合数据说明CO比N2活泼的原因:
。
第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图。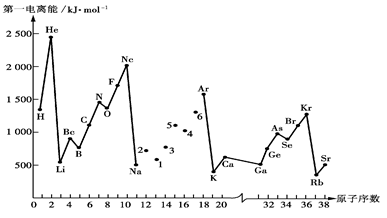
请回答以下问题:
(1)认真分析上图中同周期元素第一电离能的变化规律,将Na——Ar之间六种元素用短线连接起来,构成完整的图像。
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
。
(3)上图中6号元素在周期表中的位置是 ;其原子M层电子的轨道表示式为。
(4)上图中4,5,6三种元素的气态氢化物的沸点均比同主族上一周期的元素气态氢化物低很多,原因是:。
现有下列几种常见的物质:①N2 ②NaCl ③Ca(OH)2 ④金刚石⑤SiC ⑥NH3
⑦NH4Cl ⑧CO2。其中,(以下空格均填写序号)
(1)含有非极性键的分子晶体是;
(2)含有极性键的分子晶体是;
(3)只含离子键的离子晶体是;
(4)含有极性共价键的原子晶体是;
(5)既含有离子键,又含有极性共价键和配位键的离子晶体是 。
某链烃A的分子式为C6H12,已知其分子中所有的碳原子共平面,且该分子的一氯取代物只有一种,回答下列问题:
(1)A的结构简式为:下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量相同的是(填序号)。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
(2)A与Br2的CCl4溶液反应生成B, B与NaOH的醇溶液共热可得到D,D分子中无溴原子。请写出由B制备D的化学反应方程式:。
(3)B与足量NaOH水溶液完全反应,生成有机物E。
①E可能发生的反应类型有(填序号)。
a.取代反应 b.消去反应 c.加聚反应 d.还原反应
②E与乙二醇的关系是(填序号)。
a.同分异构体 b.同系物 c.同一物质 d.同素异形体
(4)E与乙二酸在一定条件下生成分子式为C8H12O4的有机物,请写出该反应的化学反应方程式。