已知一定条件下,单质X、Y、Z与化合物甲、乙之间存在如下变化关系:
(1)若X是O2,Y是S,Z是H2,化合物甲是一种可燃性气体,则化合物甲是
,化合物乙是 。
(2)若X是Mg,Y是C,Z是O2,化合物甲是一种不可燃气体,则化合物甲是 ,化合物乙是 。
(14分) 常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度(mol/L) |
NaOH物质的量浓度(mol/L) |
混合后溶液的pH |
| 甲 |
0.2 |
0.2 |
pH = a |
| 乙 |
C1 |
0.2 |
pH = 7 |
| 丙 |
0.2 |
0.1 |
pH >8 |
| 丁 |
0.1 |
0.1 |
pH = 9 |
请回答
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a来说明HA是强酸还是弱酸。
__________________________________________ _____________________________________。
_____________________________________。
(2)不考虑其他组的实验结果,单从乙组情况分析,C1是否一定等于0.2 mol/L________ ,混合后溶液中离子浓度c(A-)和c(Na+)的大小关系是c(A-)_______ c(Na+) (填>、<、=)。
(3)从丙组实验结果分析,HA是_______酸(强、弱),该混合液中的离子浓度由大到小的顺序是______________________________________
(4)丁组混合液中,由水电离的c(H+) =mol·L-1,c (Na+)-c (A-)=mol·L-1;
(5)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH7 (填>、<、= );
(6)将相同温度下相同浓度的四种盐溶液:
A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按c(NH4+)由大到小的顺序排列(填序号)
(17分) 重庆有丰富的天然气资源。以天然气为原料合成氨的主要步骤如下图所示(图中某些转化步骤及生成物未列出):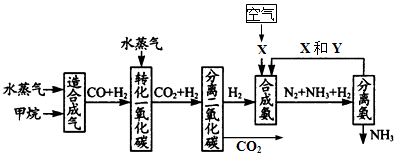
请填写下列空白:
(1)已知2mol甲烷与水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量,该反应的热化学方程式是_______________________________。
(2)图中X为_____,Y为_____(填化学式);常用K2CO3溶液吸收分离出的CO2,其离子方程式为_____________________________________
(3)在合成氨工业中,常采取的措施之一是:将生成的氨从混合气体中及时分离出来。请运用化学平衡的观点说明采取该措施的理由:_______________________________。
(4)联合制碱法中,合成氨产生的NH3与CO2通入饱和食盐水最终可制得纯碱,如图所示
①应先向食盐水通足量_______气体(写化学式,后同);副产品Z为______,可用作______;W为_______。
②若生产 Na2CO3 5.3吨,理论上至少可制得副产品Z_______吨。
(10分)向一个固定体积的密闭容器充入2 mol A和1 mol B,发生如下反应:
2A(g) + B(g) 3C(g) + D(g),2分钟后,反应达到平衡,C的浓度为1.2 mol/L。
3C(g) + D(g),2分钟后,反应达到平衡,C的浓度为1.2 mol/L。
(1)用A表示2分钟内平均反应速率,A在第1分钟平均速率第2分钟平均速率(填“<”、“>”、“=”)。
(2)器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为________(填“吸热”或“放热”)反应。
(3)大B的转化率,可采取的措施是_________(用序号填空)
①加入A②加入B③加压④再加入1.6 mol A+ 0.8 mol B⑤将C分离出容器
(4)体积可变,维持容器压强和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是_________(用序号填空)
①4 mol A + 2 mol B②3mol C + 1 mol D + l mol B
③3 mol C + 2 mol D④1.6 mol A+ 0.8 mol B + 0.6 mol C + 0.2 mol D
(12分) (1) 腐蚀电路板的反应为:Cu+2FeCl3=CuCl2+2FeCl2,
①根据该反应设计一个原电池,在方框中画出该原电池装置图,注明电极材料和电解质溶液
②负极反应式;
正极反应式。
(2) 利用电化学原理将CO、SO2转化为重要化工原料,装置如图所示:
①若A为CO,B为H2, C为CH3OH,则通入CO的一极为_____极(填“正”或“负”)。
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为:______________________________________________。
(8分) 常温下,取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(忽略体积的变化),测得混合溶液的pH=9。试回答以下问题:
(1)液的pH=9的原因是_________________________(用离子方程式表示);
(2)混合后的溶液中由水电离出的c(OH-)为a,pH=9 的NaOH溶液中由水电离出的c(OH-)为b,则ab(填“>”、“<”或“=”),a︰b=。
(3)在混合溶液中c(HA) + c(A-) = mol/L。