在2008 年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
 (1)该融雪剂的化学式是 ;Y的最高价氧化物的水化物中含有的化学键是 。
(1)该融雪剂的化学式是 ;Y的最高价氧化物的水化物中含有的化学键是 。 (2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为 。
(2)元素D原子的最外层电子数是其电子层数的2倍,且D与Y相邻;E是短周期最活泼的金属元素,试用电子式表示D与E组成化合物的形成过程为 。 (3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。
(3)元素W与Y同周期,其氧化物可作为太阳能电子板的材料;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是________ _________。 (4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为:
(4)W的氧化物是玻璃的主要成分,易与烧碱反应,该反应的化学方程式为: _______________________ ______________________。
_______________________ ______________________。
二氧化锰是制造锌锰干电池的基本材料.工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下: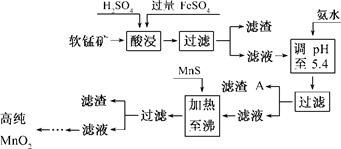
某软锰矿的主要成分为MnO2,还含Si(16.27%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物.部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
| 沉淀物 |
pH |
| Al(OH)3 |
5.2 |
| Fe(OH)3 |
3.2 |
| Fe(OH)2 |
9.7 |
| Mn(OH)2 |
10.4 |
| Cu(OH)2 |
6.7 |
| Zn(OH)2 |
8.0 |
| CuS |
≥-0.42 |
| ZnS |
≥2.5 |
| MnS |
≥7 |
| FeS |
≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为______________________________.
(2)滤渣A的主要成分为________.
(3)加入MnS的目的是除去________杂质.
(4)碱性锌锰干电池中,MnO2参与的电极反应方程式为__________________________.
(5)从废旧碱性锌锰干电池中可以回收利用的物质有________(写出两种).
在玻璃圆筒中盛有两种无色的互不相溶的中性液体,上层液体中插入两根石墨电极,圆筒内还放有一根下端弯成环状的玻璃搅棒,可以上下搅动液体,装置如右图.接通电源,阳极周围的液体呈现棕色,且颜色由浅变深,阴极上有气泡生成.停止通电,取出电极,用搅棒上下剧烈搅动.静置后液体又分成两层,下层液体呈紫红色,上层液体几乎无色.根据上述实验回答: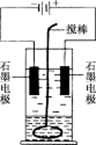
(1)阳极上的电极反应式为________.
(2)阴极上的电极反应式为________.
(3)原上层液体是________.
(4)原下层液体是________.
(5)搅拌后两层液体颜色发生变化的原因是__________________________________.
(6)要检验上层液体中含有的金属离子,其方法是______________________________,现象是__________________________________.
甲、乙两池的电极材料都是铁棒与碳棒(如下图).请回答下列问题: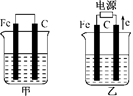
(1)若两池中均盛放CuSO4溶液,反应一段时间后:
①有红色物质析出的是:甲池中的________棒;乙池中的________棒.
②在乙池中阴极的电极反应式是________________.
(2)若两池中均盛放饱和NaCl溶液,反应一段时间后:
①写出乙池中发生的总反应的离子方程式____________________.
②将湿润的淀粉KI试纸放在乙池附近,发现试纸变蓝,待一段时间后又发现蓝色褪去,这是因为过量的Cl2将生成的I2氧化.若反应的Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为____________________.
③若乙池转移0.02 mol电子后停止实验,池中溶液的体积是200 mL,则溶液混匀后的pH=________.
工业上处理含Cr2O72—的酸性工业废水常用以下方法:①往工业废水里加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀产生;③过滤回收沉淀,废水达到排放标准.试回答:
(1)电解时的电极反应:阳极________________,阴极__________________________.
(2)Cr2O72—转变成Cr3+的离子反应方程式:_____________________.
(3)电解过程Cr(OH)3、Fe(OH)3沉淀是怎么产生的?
______________________________________.
(4)能否用Cu电极来代替Fe电极?________(填“能”或“不能”),简述理由______________________.
.短周期元素D、E、X、Y、Z原子序数逐渐增大。它们的最简氢化物分子的空间构型依次是正四面体、三角锥形、正四面体、角形(V形)、直线形。回答下列问题:
(1)Y的最高价氧化物的化学式为______;Z的核外电子排布式是_______。
(2)D的最高价氧化物与E的一种氧化物为等电子体,写出E的氧化物的化学式。
(3)D和Y形成的化合物,其分子的空间构型为____________;D原子的轨道杂化方式是____________。X与Z构成的分子是________分子(填“极性”或“非极性”)
(4)写出一个验证Y与Z的非金属性强弱的离子反应方程式___________。
(5)金属镁和E的单质在高温下反应得到的产物与水反应生成两种碱性物质,该反应的化学方程式是__________________________________________。