(6分)"比较"是化学研究物质性质的基本方法之一,请运用比较法解答下列问题
已知在一定条件下,过氧化钠几乎可与所有的常见气态非金属氧化物反应。
如:2Na2O2+2CO2=2Na2CO3+O2,Na2O2+CO=Na2CO3。
(1)试分别写出Na2O2与SO2、SO3反应的化学方程式。

(2)当1molSO3参加反应时,转移电子的物质的量为 mol。
(3)通过比较可知:在氧化物中,当非金属元素处于 价时,其氧化物与过氧化钠反应就有O2生成 。
。
工业上利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制备高档颜料铁红(Fe2O3),具体生产流程如下:
试回答下列问题:
(1)滤液X中含有的金属阳离子是____ ___(填离子符号)。
(2)步骤Ⅲ中可选用________调节溶液的pH(填选项字母)。
| A.稀硝酸 | B.氨水 | C.氢氧化钠溶液 | D.高锰酸钾溶液 |
(3)步骤Ⅳ中,FeCO3沉淀完全后,溶液中含有少量Fe2+,检验Fe2+的方法是________。
(4)步骤Ⅳ的反应温度一般需控制在35℃以下,其目的是_________,_______。
(5)在空气中煅烧FeCO3生成产品氧化铁的化学方程式为______________________。
某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 |
CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 |
Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。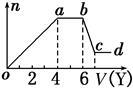
(1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是_____ ,___,ab段发生反应的离子是________,bc段发生反应的离子方程式为__________。
(2)若Y是NaOH溶液,则X中一定含有的阳离子是_____ ,__ _,其物质的量之比为_________,ab段反应的离子方程式为____________。
【化学选修5有机化学基础】2011年4月台湾曝出的增塑剂风波一度让人们“谈塑色变”。常用的增塑剂如下:
请回答下列问题:
(1)下列对甲的叙述正确的是 (填选项字母)
| A.甲能使Br2的CCl4溶液退色 |
| B.甲的单体是CH3CH = CHCOOCH2CH2CH3 |
| C.1 mol甲能与1 mol NaOH发生水解反应 |
| D.甲能发生酯化反应、取代反应、消去反应、加成反应 |
(2)丙中含有的官能团名称是 。
(3)乙的同分异构体有多种,写出其中一种不含甲基的羧酸的结构简式 。
(4)已知通过燃烧法确定丁的含氧量(质量分数)为23%。以某烃A为原料合成该塑料增塑剂的流程如下:
①反应1的反应条件是 。
②反应2的反应类型是 。
③反应3的化学方程式是 。
【化学选修3物质结构与性质】有X、Y、Z、W、P、Q六种前两周期的主族元素,原子序数依次增大,价电子数之和为26,原子半径依Y、Z、W、P、Q、X依次减小。围绕上述元素,回答下列问题:
(1)Q的电子排布图为 ,YQ3中心原子的杂化类型为 ,除X外,其余元素的第一电离能由小到大顺序为 (元素符号回答)。
(2)X2P和ZP2固态时均为分子晶体,但熔点X2P比ZP2高得多,原因是 。
(3)固体A是离子晶体,结构类似于CsCl,组成中含W的质量分数为73.7%,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,该物质适当加热就分解成两种单质气体。该物质的电子式 ,其与水反应的化学方程式为 。
(4)Z单质有三类异形体,其中一种骨架型原子晶体的立方晶胞如图,计算晶体中Z原子的空间利用率为 ( )。
)。
节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若宁波全市的140余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨。甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2 CH3OH。请根据图示回答下列:
CH3OH。请根据图示回答下列:
(1)关于该反应的下列说法中,正确的是 (填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,净测得CO和CH3OH(g)的浓度随时间变化如(图1)所示。从反应开始到平衡,CO的平均反应速率v(CO)= ,该反应的平衡常数K= 。
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有 。
A.升高温度B.充入He气
C.再充入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量=_____g/mol。
(5)根据(图2),写出此反应的热化学方程式 。