(16分)已知:RCH=CH2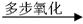 RCH2COOH,下图表示有机物A、B、C、D、E、F、X、Y之间的转变关系:
RCH2COOH,下图表示有机物A、B、C、D、E、F、X、Y之间的转变关系:
其中:X、Y互为同分异构体,F和C互为同系物,E和D互为同系物,B中含支链,且核磁共振氢谱测得有3个吸收峰,峰高6:1:1;A的密度在标准状况下为1.25g/L;A、B、X、Y的分子式都符合CnH2nO0. 5n-1
(1)B的结构简式为 ,Y的结构简式为
(2)C和D生成X的化学反应类型为
A、加成反应 B、消去反应
C、取代反应 D、酯化反应
(3)实验室制取A的化学反应方程式为 ;
(4)实验室组装A的发生装置时,用到的玻璃仪器主要有酒精灯、导气管
(5)收集A的装置是 (填序号)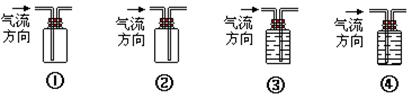
(6)实验室制取A时,常因温度过高而生成有刺激性气味的气体e,设计一个简单的实验以验证发生装置中生成的A有还原性,可使产生气体依次通过下列溶液中的一种或几种,则所选试剂的顺序为 (填序号,可不全选,也可以重复使用)
①品红溶液 ②溴水
③氢氧化钠溶液 ④酸性高锰酸钾溶液
现有m g某气体,它是由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数的数值用NA表示,则:
(1)该气体的物质的量为mol。
(2)该气体所含原子总数为个。
(3)若该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为。
(4)若该气体溶于1L水后所得溶液的密度为ρ g·cm-3,其物质的量浓度为mol/L。
取20ml 5mol/LNaOH溶液,加水稀释成100ml,所得溶液的物质的量浓度为;欲中和50ml稀释后的溶液,需2.5mol/LH2SO4溶液ml。
(1)用20g烧碱配制成500mL溶液,其物质的量浓度为mol/L;从中取出1mL,其物质的量浓度为mol/L;含溶质g;若将这1mL溶液用水稀释到100mL,所得溶液的物质的量浓度为mol/L,其中含Na+g。
(2)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为,R的相对原子质量为。
(1)在V L Al2(SO4)3溶液中,测得含Al3+的质量为a g,则Al2(SO4)3溶液的物质的量浓度为,SO42-的物质的量浓度为。
(2)在标准状况下,4 g H2、11.2 L O2、1 mL H2O中,所含分子数最多的是,含原子数最多的是,质量最大的是,体积最小的是。
(3)在同温同压下,同体积的甲烷(CH4)和二氧化碳分子数之比为,物质的量之比为,原子总数之比为,质量之比为 ,密度之比为 。
某原电池构造如下图所示。其电池的总反应是:Cu(s) + 2Ag+ (aq) = Cu2+ (aq) + 2Ag(s)。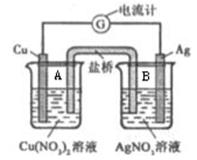
请回答以下问题:
(1)若盐桥为琼脂-KOH组成,其作用是___________________________。OH-离子移向_______(填“A”或“B”)中的溶液。Cu为原电池的______极,其电极反应式是_____________________________。A中的电解质溶液在该电池工作一段时间后会出现_______________________的现象。
(2)把盐桥改为铁棒后,电流计的指针 (填“会”、“不会”)发生偏转,A装置名称 (填“原电池”或“电解池”),铜棒的电极名称为 (填“正极”、“负极”、“阴极”或“阳极”)(提示:当两个原电池串联时,电极材料的金属活动性相差较大的为原电池,电极材料的金属活动性相差较小的为电解池)。
(3)把盐桥改为铜棒后,电流计的指针 (填“会”、“不会”)发生偏转,左边烧杯中的硝酸铜浓度 (填“增大”、“减小”或“不变”)
(4)把盐桥改为银棒后,电流计的指针 (填“会”、“不会”)发生偏转,理由是 。