|
将标准状况下的 a LHCl(气)溶于100g水中,得到的盐酸密度为bg· cm—3,则该盐酸的物质的量浓度是
A.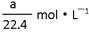 |
B.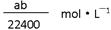 |
C. |
D.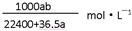 |
下列说法正确的是()
| A.营养学家编制的大众食谱不一定对每个人都适用 |
| B.靠不吃或少吃减肥是不正确的,有害健康 |
| C.每一种食物含有多种营养素,因此偏食不会影响身体健康 |
| D.人体缺少维生素C容易得甲亢 |
下列离子方程式书写正确的是()
| A.铜跟稀硝酸反应:3Cu+ 8H++2NO3-=3Cu2++2NO↑+4H2O |
| B.硫酸与氢氧化钠混合:H++OH-=H2O |
| C.金属铁与稀硫酸反应:2Fe+6H+=2Fe3+ + 3H2↑ |
| D.铜与氯化铁溶液反应:Fe3++Cu═ Fe2++Cu2+ |
下列反应属于氧化还原反应的是()
| A.浓盐酸与二氧化锰共热 | B.石灰石与稀盐酸反应 |
| C.氯化钠溶液与硝酸银溶液反应 | D.氯化亚铁与稀硝酸反应 |
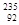 U是重要的核工业原料,下列有关
U是重要的核工业原料,下列有关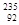 U说法正确的是()
U说法正确的是()
A.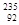 U原子核中含有143个中子 U原子核中含有143个中子 |
B.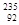 U原子核外有143个电子 U原子核外有143个电子 |
C.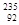 U与 U与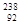 U互为同位素 U互为同位素 |
D.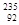 U与 U与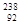 U互为同素异形体 U互为同素异形体 |
某有机物的结构简式为CH2=CH—COOH,该化合物可能发生的化学反应是()
| A.水解反应 | B.加聚反应 | C.消去反应 | D.酯化反应 |