在指定溶液中,下列各组离子一定能大量共存的是: ( )
A.pH=1的溶液: |
B.由水电离出的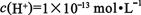 的溶液: 的溶液: |
C.含大量Fe3+的溶液: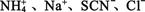 |
D.pH=13的溶液: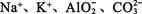 |
下列说法或表示方法中正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.由C(金刚石) = C(石墨) ΔH= -1.9 kJ·mol-1可知,金刚石比石墨稳定 |
| C.在101 Kpa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:2 H2(g)+O2(g) =" 2" H2O(l) ΔH =" +285.8" kJ·mol-1 |
| D.稀溶液中:H+(aq) + OH-(aq) = H2O(l) ΔH = -57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
已知:P4(s.白磷)+5O2(g)= P4O10(s)△H =-2983.2 kJ·mol-1
4P(s.红磷)+5O2(g)= P4O10(s)△H =-2954 kJ·mol-1
那么,1mol红磷转变成相应物质的量白磷时,应是
| A.吸收29.2 kJ热量 | B.放出29.2 kJ热量 |
| C.放出7.3 kJ热量 | D.吸收7.3 kJ热量 |
已知热化学方程式:SO2(g)+ 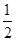 O2(g)
O2(g)  SO3(g)△H =" ―98.32" kJ·mol-1,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
SO3(g)△H =" ―98.32" kJ·mol-1,在容器中充入2molSO2 和1molO2充分反应,最终放出的热量为
| A.196.64 kJ | B.196.64 kJ·mol-1 | C.<196.64 kJ | D.>196.64 kJ |
下列各图所表示的反应是吸热反应的是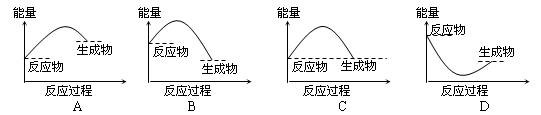
N2H4是一种高效清洁的火箭燃料。0.25 mol N2H4(g)完全燃烧生成氮气和气态水时,
放出133.5 kJ热量。则下列热化学方程式中正确的是( )
A.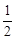 N2H4(g)+ N2H4(g)+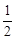 O2(g)==== O2(g)====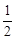 N2(g)+H2O(g);ΔH=+267 kJ·mol-1 N2(g)+H2O(g);ΔH=+267 kJ·mol-1 |
| B.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH =-534 kJ·mol-1 |
| C.N2H4(g)+O2(g)====N2(g)+2H2O(g);ΔH =+534 kJ·mol-1 |
| D.N2H4(g)+O2(g)====N2(g)+2H2O(l);ΔH =-133.5 kJ·mol-1 |