有X、Y、Z、W四种金属。已知X的最高价氧化物的水化物的碱性比Y的强;X3+可使Z氧化;W可与热水反应产生H2,X不能与热水反应;把X的金属片插入稀H2SO4中,让金 属丝Z与X接触,则X的溶解速率加快
属丝Z与X接触,则X的溶解速率加快 。这四种金属活动性强弱关系一定是:
。这四种金属活动性强弱关系一定是:
| A.Y>X | B.Z>Y | C.W>Z | D.Z>X |
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4 mol/L和2 mol/L,取10 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反应中HNO3被还原成NO)
| A.0.448 L | B.0.672 L | C.0.896 L | D.0.224 L |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示。下列说法正确的是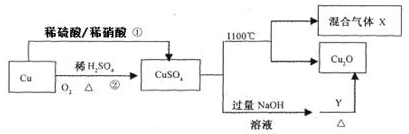
| A.途径①和途径②都体现了硫酸的酸性和氧化性 |
| B.Y可以是酒精溶液 |
| C.CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D.将CuSO4溶液蒸发浓缩、冷却结晶,可制得胆矾晶体 |
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是
| A.取a克混合物充分加热,减重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体。 |
在酸性条件下,向含有铬废水中加入FeSO4,可将有害的Cr2O72-转化为 Cr3+,然后再加入熟石灰调节溶液的pH,使Cr3+转化为Cr(OH)3沉淀,而从废水中除去.下列说法正确的是
| A.FeSO4在反应中作氧化剂 |
| B.随着反应的进行,该废水的pH会减小 |
| C.若该反应转移0.6mol e-,则会有0.2mol Cr2O72-被还原 |
| D.除去废水中含铬元素离子的过程包括氧化还原反应和复分解反应 |
下列有关元素周期表和元素周期律的说法中,正确的是
| A.第三周期主族元素中氯的原子半径最大 |
| B.原子最外层电子数为2的元素一定位于周期表中的第ⅡA族 |
| C.同主族自上而下,其非金属元素气态氢化物的稳定性逐渐增强 |
| D.镓(Ga)位于第4周期、ⅢA族,其最高价氧化物对应水化物的化学式为Ga(OH)3 |