《硫酸铜晶体里结晶水含量的测定》是中学化学中的重要实验,请回答下列该实验的相关问题。
(1)实验中能直接加热的仪器名称为____________;进行的称量操作至少为________次。
(2)下列操作会引起测定结果偏高的是__________________
| A.加热时温度过高CuSO4发生分解 | B.加热后在空气中冷却再称量 |
| C.加热过程中有晶体溅出 | D.晶体部分风化 |
某烧碱样品含有少量不与酸作用的杂质,为了滴定其纯度,进行以下滴定操作:
A.在250mL的容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中滴加几滴酚酞做指示剂
C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为C的标准盐酸溶液装入酸式滴定管,调整液面记下开始读数为V1mL
E.在锥形瓶下垫一张白纸,滴定至红色刚好消失为止,且颜色不再变化,记下读数V2mL
回答下列问题:
(1)正确操作步骤的顺序是(填字母):→→→ D →。
(2)操作E中的锥形瓶下垫一张白纸的作用是。
(3)操作D中液面应调整到,尖嘴部分应。
(4)某学生实验时把锥形瓶用烧碱溶液润洗,使测定的浓度(填“偏高”、“偏低”或“无影响”),原因是。
(5)当用酸滴定碱时,下列操作中使测定结果(碱的浓度)偏低的是。
A.酸式滴定管滴至终点时,俯视读数
B.碱液移入锥形瓶后,加了10 ml蒸馏水再滴定
C.酸式滴定管用蒸馏水润洗后,未用操作液润洗
D.酸式滴定管注入酸液后,尖嘴留有气泡,开始滴定
(6)该烧碱样品纯度的计算式为。
某化学兴趣小组利用浓盐酸、二氧化锰共热制氯气,并用氯气和消石灰制取少量漂白粉。现已知反应:2Cl2+2Ca(OH)2 = Ca(ClO)2+CaCl2+2H2O,该反应是放热反应,温度稍高即发生副反应。试回答以下问题: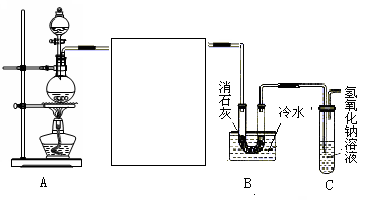
(1)制取氯气时在烧瓶中加入一定量的二氧化锰,通过(填仪器名称)向烧瓶中加入适量的浓盐酸,写出该反应的离子方程式。
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内(示意图),并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是。
(3)实验室若用16 mol •L-1的盐酸100 mL与足量的二氧化锰反应,理论上最终生成的Ca(ClO)2的物质的量最多不超过mol。
(14分)设计一个简单的一次性完成实验的装置图,目的是验证醋酸溶液,二氧化碳水溶液、苯酚溶液的酸性强弱顺序。
①利用上图所示的仪器可以组装实验装置,则仪器的连接顺序为:
接_____ , 接______ ,接(填字母)
②写出装置I和II中的实验现象:
I中;II中
③写出装置II中发生反应的方程式
④由强到弱排序三者的酸性顺序
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是氯气能与水作用形成具有________性的次氯酸,相关反应的离子方程式为________________________;
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8∶00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5 mg/L至1.0 mg/L 之间时,效果最好。上图是该小组测定的每天19∶00时游泳池中水的含氯量,有哪几天使用游泳池不卫生_________________:
(3)你认为哪几天的天气炎热、阳光强烈________,说出一种理由是____________ ____________;
(4)在对游泳池水中通入氯气消毒时,当发生氯气泄漏,应立即关闭氯气罐,还应采取下列自救方法________。(选填序号)
| A.用湿润的毛巾捂住口鼻跑向低处 |
| B.用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处 |
| C.用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处 |
| D.用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处 |
(5)小型游泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液而非氯气消毒的一项理由________________________。
酯类是工业上重要的有机原料,具有广泛用途。
下图是乙酸乙酯的合成路线图,已知A能与银氨溶液反应析出银镜,B的水溶液可以溶解CaCO3,E可作果实催熟剂。
请完成下列问题:
(1)A的名称是________;B中所含的官能团是________;反应③的类型是;反应④的类型是。
(2)A的结构简式为________;E的结构简式为________。
(3)请写出反应③、④的化学方程式:③________;④________。
(4)请写出CH3COOCH2CH3的酯类物质的同分异构体的结构简式(写两种即可)。