下列粒子的结构示意图中,表示硫原子的是
对于任何一个平衡体系,采取以下措施,一定使平衡发生移动的是( )
| A.加入一种反应物 | B.增大体系的压强 |
| C.升高温度 | D.使用催化剂 |
取五等份NO2,分别通入温度不同、容积相同的恒容密闭容器中,发生反应:
2NO2(g)  N2O4(g) ,H<0,反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随温度(T)变化关系图。下列示意图中,最可能与实验结果相符的是( )
N2O4(g) ,H<0,反应相同时间后,分别测定体系中NO2的百分含量(NO2%),并作出其随温度(T)变化关系图。下列示意图中,最可能与实验结果相符的是( )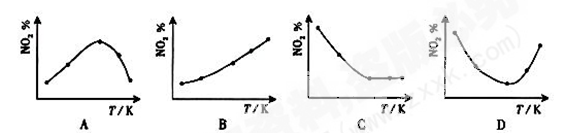
常温下,下列关于电解质溶液的判断正确的是( )
| A.在pH=12的溶液中,K+、Cl-、HCO3-、Na+可以常量共存 |
| B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以常量共存 |
| C.0.1 mol/L一元碱BOH溶液的pH=10,可推知BOH溶液中存在BOH = B++OH- |
D.在0.1 mol/L一元酸HA溶液的pH=3,可推知NaA溶液中存在:A-+H2O HA+OH- HA+OH- |
HA为酸性略强于醋酸的一元弱酸,在0.1 mol/L NaA溶液中,离子浓度关系正确的是( )
| A.c(Na+)>c(A-)>c(H+)>c(OH-) |
| B.c(Na+)>c(A-)>c(OH-)>c(H+) |
| C.c(Na+)+c(OH-) = c(A-)+c(H+) |
| D.c(Na+)+c(H+) = c(A-)+c(OH-) |
恒温下,反应aX(g)  bY(g)+cZ(g),达到平衡状态。若把容器的体积压缩到原来的
bY(g)+cZ(g),达到平衡状态。若把容器的体积压缩到原来的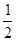 ,达到平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L。下列判断正确的是( )
,达到平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L。下列判断正确的是( )
| A.a>b+c | B.a=b+c | C.a<b+c | D.a=b=c |