在右图所示的原电池中,负极发生的反应是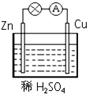
| A.Cu2+ + 2e- ="=" Cu | B.Cu-2e- ="=" Cu2+ |
| C.2H+ + 2e- ="=" H2↑ | D.Zn-2e- ="=" Zn2+ |
下图中a、b、c、d、e为周期表前4周期的一部分元素,有关叙述正确的是
| A.b元素除0价外,只有一种化合价 |
| B.c元素只能形成一种氢化物且很不稳定 |
| C.d元素是五种元素中原子半径最小的一种 |
| D.e元素最高价氧化物的水化物和不同量的氢氧化钠溶液反应,可能生成三种盐 |
设阿伏加德罗常数为NA,下列叙述中正确的是
| A.1 mol 18O2所含质子数为16NA |
| B.10 g氖气所含原子数为0.5NA |
| C.0.5 mol Al和足量烧碱反应转移的电子数为1.5NA |
| D.标准状况下11.2 L SO3所含分子数为0.5NA |
向FeI2溶液中不断通入Cl2,溶液中I-、I2、IO3-、Fe2+、Fe3+等粒子物质的量随n(Cl2)/n(FeI2)(即Cl2与FeI2的物质的量之比)的变化可用下图简单表示(“—”表示铁各种价态的变化,用“—·—”表示碘各种形态的变化)。
据此得出的下列结论中错误的是
| A.I-、Fe2+、I2的还原性和Cl2、Fe3+、I2的氧化性都依次减小 |
| B.当n(Cl2)/n(FeI2)==1.2时,离子方程式为2Fe2++10I-+6Cl2==5I2+2Fe3++12Cl- |
| C.当n(Cl2)/n(FeI2)==6.5时,溶液中n(Cl-)/n(IO3-)==6.5 |
| D.若溶液体积不变,溶液的pH始终不变 |
三聚氰胺俗称蜜胺,主要用于生产三聚氰胺一甲醛树脂。三聚氰胺微溶于冷水,易结晶,可溶于热水,低毒。在一般情况下较稳定,但在高温下可能会分解放出氰化物。其结构式如右图,下列有关说法不正确的是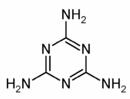
| A.用三聚氰胺制造的餐具不可以放进微波炉中加热使用 |
| B.长期摄入三聚氰胺会造成生殖、泌尿系统的损害,使膀胱、肾部结石 |
| C.该化合物属于芳香烃 |
| D.三聚氰胺呈弱碱性,可与盐酸、硫酸等酸反应形成三聚氰胺盐 |
右图表示金属X、Y以及它们的合金Z分别与足量盐酸反应时产生氢气的情况,其中横坐标表示消耗金属的物质的量,纵坐标表示产物氢气的体积(标准状况)。下列对有关Z的组成的判断,正确的是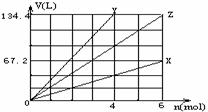
| A.n(Na):n(Fe)="2:1" | B.n(Mg):n(K)="1:2" | C.n(Na):n(Al)="1:3" | D.n(K):n(Al)="1:1" |