已知:H2(g)+F2(g)===2HF(g);ΔH=-270 kJ/mol,下列说法正确的是: ( )
| A.氟化氢气体分解生成氢气和氟气的反应是放热反应 |
| B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ |
| C.在相同条件下1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 |
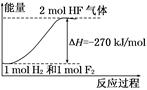
| D.该反应中的能量变化可用下图来表示 |
在高压下,用激光器加热到1800 K时,人们成功制得了原子晶体——干冰,下列推断正确的是()
| A.该干冰晶体有很高的熔点和沸点 | B.该干冰晶体可用作制冷材料 |
| C.该干冰晶体和石英一样可用作耐磨材料 | D.该干冰晶体中的键角是180° |
在医院施行外科手术时,常用HgCl2的稀溶液作为手术刀的消毒剂。已知HgCl2有如下性质:①HgCl2晶体熔点较低;②HgCl2在熔融状态下不能导电;③HgCl2在水溶液中可发生微弱的电离。下列关于HgCl2的叙述正确的是( )
| A.HgCl2属于共价化合物 | B.HgCl2属于离子化合物 |
| C.HgCl2属于非电解质 | D.HgCl2属于强电解质 |
关于下列说法正确的是( )
| A.加热氯化铵与固化碘过程中发生的都是升华 |
| B.氢键的存在主要影响物质的物理性质,如熔沸点和在水中的溶解度 |
| C.水分子相当稳定是因为水分子间存在很强的分子间作用力 |
| D.直接由原子构成的晶体必然是原子晶体 |
下列数据是对应物质的熔点(℃):
| NaCl |
Na2O |
AlF3 |
AlCl3 |
BCl3 |
Al2O3 |
CO2 |
SiO2 |
| 801 |
920 |
1291 |
190 |
-109 |
2073 |
-57 |
1723 |
据此作出的下列判断,错误的是( )
| A.铝的化合物的晶体中有离子晶体 | B.只有BCl3、干冰是分子晶体 |
| C.同族元素的氧化物可形成不同类型的晶体 | D.不同族元素的氧化物可形成相同类型的晶体 |
为了确定SbCl3、SbCl5、SnCl4是否为离子化合物,可以进行下列实验,其中合理、可靠的是( )
| A.观察常温下的状态,SbCl5是苍黄色液体,SnCl4为无色液体。结论:SbCl5和SnCl4都是离子化合物 |
| B.测定SbCl3、SbCl5、SnCl4的熔点依次为73.5 ℃、2.8 ℃、-33 ℃。结论:SbCl3、SbCl5、SnCl4都不是离子化合物 |
| C.将SbCl3、SbCl5、SnCl4溶解于水中,滴入HNO3酸化的AgNO3溶液,产生白色沉淀。结论:SbCl3、SbCl5、SnCl4都是离子化合物 |
| D.测定SbCl3、SbCl5、SnCl4的水溶液的导电性,发现它们都可以导电。结论:SbCl3、SbCl5、SnCl4都是离子化合物 |