下列离子方程式中正确的是 ( )
A.向NaHSO4溶液中滴加Ba( OH)2至SO42-沉淀完全2H+ + SO42- + Ba2+ + 2OH- = BaSO4↓+ 2H2O OH)2至SO42-沉淀完全2H+ + SO42- + Ba2+ + 2OH- = BaSO4↓+ 2H2O |
| B.碳酸钠溶液与醋酸反应:CO32- + 2H+ = CO2↑+ H2O |
C.氢氧化亚铁与硝酸混合:Fe(OH)2 + 2H+ = Fe2+ +  2H2O 2H2O |
| D.将1~2mL氯化铁饱和溶液加到20mL沸水中:Fe3+ + 3H2O = Fe(OH)3(胶体) + 3H+ |
以NA代表阿伏伽德罗常数,则关于热化学方程式C2H2(g)+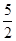 O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ/mol的说法中,正确的是( )
O2(g)===2CO2(g)+H2O(l) ΔH=-1300 kJ/mol的说法中,正确的是( )
| A.当12NA个电子转移时,该反应放出1300 kJ的能量 |
| B.当1NA个水分子生成且为液体时,吸收1300 kJ的能量 |
| C.当有2NA个碳氧共用电子对生成时,放出1300 kJ的能量 |
| D.当有8NA个碳氧共用电子对生成时,放出1300 kJ的能量 |
在密闭容器中发生如下反应:xA(g)+yB(g) zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是()
zC(g),达到平衡后测得A的浓度为0.20mol/L。在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L。下列说法不正确的是()
| A.x+y﹥z | B.平衡向右移动 | C.B的转化率提高 | D.C的体积分数降低 |
航天燃料从液态变为固态,是一项技术突破。铍是高效率的火箭材料,燃烧时放出巨大的能量,每千克的铍完全燃烧放出的热量为62 700 kJ。则铍燃烧的热化学方程式正确的是( )
A.Be+ O2===BeO ΔH=-564.3 kJ·mol-1 O2===BeO ΔH=-564.3 kJ·mol-1 |
B.Be(s)+ O2(g)===BeO(s)ΔH=+564.3 kJ·mol-1 O2(g)===BeO(s)ΔH=+564.3 kJ·mol-1 |
C.Be(s)+ O2(g)===BeO(s)ΔH=-564.3 kJ·mol-1 O2(g)===BeO(s)ΔH=-564.3 kJ·mol-1 |
D.Be(s)+ O2(g)===BeO(g) ΔH=-564.3 kJ O2(g)===BeO(g) ΔH=-564.3 kJ |
右图是关于反应A2(g)+3B2(g)===2C(g)△H<0的平衡移动图形,影响平衡移动的原因是()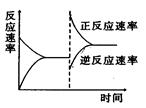
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时使用催化剂; |
| D.增大反应物浓度,同时减小生成物浓度 |
对于3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )