用NA代表阿伏加德罗常数的值,下列有关说法正确的是 ( )
| A.78g过氧化钠晶体中,含2NA个阴离子 |
| B.常温常压下,22.4L氦气含有NA个氦原子 |
| C.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA |
| D.常温下16g O2与O3的混合气体中含氧原子数为NA |
设NA表示阿伏加德罗常数的值。下列说法中正确的是
| A.5.6 g Fe和一定量的浓HNO3或稀硝酸完全反应,转移电子均为0.3 NA |
| B.16 g氧气或臭氧的氧原子个数均为NA |
C.1 mol石墨或金刚石中六元环个数均为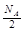 |
| D.28.6 g Na2CO3·10H2O在晶体中或溶液中,含有的CO32—离子均小于0.1 NA |
A、B、C为三种短周期元素,A、B在同周期,A、C的最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中正确的是
A.原子序数: B>A>C B.原子半径:A>B>C
C.离子半径:A2->C->B2+ D.原子核外最外层电子数:A>C>B
关于下列图示的说法中,正确的是 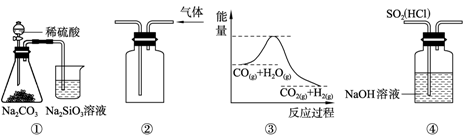
| A.图①所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
| B.用图②所示实验装置排空气法收集CO2气体 |
C.图③表示可逆反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH大于0 CO2(g)+H2(g)的ΔH大于0 |
| D.图④ 装置可以用来除去SO2中的HCl |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的几种。现取该溶液进行实验,得到如下实验现象:①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。据此可以推断,该溶液中肯定不存在的离子是
| A.Al3+、CO32-、Br-、SO32- | B.Mg2+、Na+、CO32-、I- |
| C.Al3+、Na+、SO32-、I- | D.Al3+、Mg2+、I-、SO32- |
2010年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中
钯催化交叉偶联”而获奖。钯的化合物氯化钯可用来检测有毒气体CO,发生反
应的化学方程式为:CO+PdCl2 +H2O =CO2 +Pd↓ +2HC1。
下列说法正确的是
| A.题述反应条件下还原性:CO> Pd |
| B.题述反应中PdCl2被氧化 |
| C.生成22.4 LCO2时,转移的电子为2 mo1 |
| D.CO气体只有在高温下才能表现还原性 |