设阿伏加德罗常数为NA。则下列说法正确的是 ( )
| A.7.1g Cl2与足量NaOH溶液充分反应后,转移的电子数为O.1 NA |
| B.1.0L浓度为1.0 mol·L-1的一元酸溶液中含有的氢离子数为1.0 NA |
| C.常温下,1L 0.1 mo1.L-1的NH4NO2溶液中氮原子数小于0.2 NA |
| D.标准状况下,22.4L乙醛中含有的氧原子数为1.0 NA |
25 ℃时,H2SO3 HSO3-+H+的电离平衡常数Ka=1×10-2,下列说法不正确的足
HSO3-+H+的电离平衡常数Ka=1×10-2,下列说法不正确的足
| A.该温度下NaHSO3的水解平衡常数Kb=1×10-12 |
| B.若向NaHSO3溶液中加入少量的I2,则溶液中c(H2SO3) /c(HSO3-) 将减小 |
| C.略微升高温度 Ka(H2SO3)和Kh(NaHSO3 )均增大 |
| D.NaHSO3溶液中:c(H+)<c(SO32-)+c(HSO3-)+c(OH-) |
有关化学反应的方向和速率的研究可以指导化工生产。下列说法正确的是
A.N2+3H2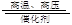 2NH3 2NH3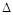 H<0,在任何温度下均为自发反应 H<0,在任何温度下均为自发反应 |
| B.向新制氯水中加入少量小苏打固体可提高其漂白能力 |
C.1 L密闭容器中发生反应4NH3+5O2 4NO+6H2O ,充人少量 N2可加快反应速率 4NO+6H2O ,充人少量 N2可加快反应速率 |
| D.湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu ,反应中的Fe可以用Na代替 |
1 mol乙烷与3 mol Cl2在光照条件下反应,理论上得到的氯代物有
| A.3种 | B.5种 | C.7种 | D.9种 |
下列离子方程式书写正确的是
| A.KMnO4溶液用盐酸酸化并加入H2O2 :2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
| B.Fe2(SO4)3和Ba(OH)2溶液混合:2Fe3++3SO42-+3Ba2++6OH-=2Fe(OH) 3↓+3BaSO4↓ |
| C.等体积等物质的量浓度的AlCl3、Ba(OH)2、HCl溶液混合:3H++Al3++6OH-=Al(OH)3↓+3H2O |
| D.水玻璃与稀醋酸混合:SiO32-+2H+=H2SiO3↓ |
下列物质的分离和鉴别方法正确的是
| A.用分液法分离碘酒和CCl4 |
| B.用饱和碳酸钠溶液萃取乙醇中的乙酸 |
| C.用银氨溶液鉴别甲酸乙酯和乙醛 |
| D.用浓溴水鉴别苯和环己烯 |