在常温下,有下列九种物质:
①石墨 H2S ③CaCO3 ④液态NH3
⑤CH3COONH4 晶体⑥CO2 ⑦Na Cl溶液 ⑧Na
⑨CH3CH2OH
请根 据要求填写下列空白:(填序号)
据要求填写下列空白:(填序号)
(1)属于非电解质的是 ;
(2)属于强电解质的 是 ;
是 ;
(3)在上述九种物质中,能导电的是 ;
(4)写出下列物质的电离方程式:H2S
(10分)某同学现要对一份废液中所含的离子作出一些判定。已知溶液中可能是含有SO42-、Na+、CO32-、HCO3—、H+、NO3-、Cu2+、Cl—等离子中的若干种。经观察知:溶液无色、澄清。然后他又作了如下的分析:
①取少量溶液,用PH试纸 检验,得PH="1" 可知该溶液有强酸性
检验,得PH="1" 可知该溶液有强酸性
②重新取原溶液,用稀HCl 和BaCl2检验该溶液,有白色沉淀生成.
③将②所得的浊液静置,取上层清液,往清液中加入少量的AgNO3溶液和稀HNO3,结果又有白色沉淀生成
可得出结论:原溶液中一定有___________离子;
一定没有离子;可能有__________离子
写出步骤②的离子反应方程式:_____________________________
写出步骤③的离子反应方程式:_____________________________
(8分) (1)利用下列反应原理可以用于检查司机是否酒后开车。
2K2Cr2O7+3C2H5OH=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O
(橙色)(酒精)(绿色)
①若司机酒后开车,检测器中的溶液显示出色
②在反应中,铬元素被___________(填“氧化”或“还原 ”)
”)
(2)一个体重50Kg的健康人,含铁2g。这2g铁在人体中不是以单质金属的形式存在的,而是以Fe2+和Fe3+的形式存在。二价铁离子易被吸收,给贫血者补充铁时,应给予含二价铁离子的二价铁盐,如硫酸亚铁(FeSO4)。服用维生素C,可使食物中的三价铁离子还原成二价铁离子,有利于铁的吸收。
这句话指出维生素C在这一反应中做 _______剂,具有性。
(1)下列物质:①CO2②盐酸③烧碱晶体④酒精⑤铁⑥纯 醋酸(用编号回答)其中属于电解质的有;属非电解质的是。
醋酸(用编号回答)其中属于电解质的有;属非电解质的是。
(2)按要求写出下列反应的离子方程式:
①铁和盐酸反应:______________________________________
②CuSO4和Ba(OH)2反应:
(1)某含碳、氢、氧三种元素的有机物,其碳、氢、氧的质量比为6:1:8,它的实验式为__________;该有机物蒸气的密度是相同条件下氢气密度的30倍,则该有机物的分子式为_______________。
(2)据报道,2002年10月26日俄罗斯特种部队在解救人质时,使用了一种麻醉作用比吗啡强100倍的氟烷,已知氟烷的化学式为C2HClBrF3,则沸点不同的上述氟烷有4种,它们的结构简式分别是:
有的油田开采的石油中溶有一种碳氢化合物——金刚烷,它的分子立体结构如图所示: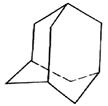
(1)由图可知其分子式为:____________。
(2)它是由_________ 个六元环构成的六体的笼状结构,其中有__________个碳原子为三个环共有。
(3)金刚烷分子 的一氯代物有_______种;二氯代物有种。
的一氯代物有_______种;二氯代物有种。