在密闭容器中,使2molN2和6molH2混合发生下列反应:
N2(g)+3H2(g)===2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是_______;N2和H2的转化率比是_________。
(2)升高平衡体系的温度(保持体积不变),混和气体的平均相对分子质量_______,密度________。(填“变大”、“变小”或“不变” )
(3)当达到平衡时,将C(N2)、C(H2)、C(NH3)同时减小一倍,平衡将向______移动。
(4)当达到平衡时,充入氩气,并保持压强不变,平衡将向_________移动。
(5)若容器恒容,绝热、加热使容器内温度迅速升至原来的2倍,平衡将_______
(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度_______(填“大于”“小于”或“等于”)原来的2倍。
萝卜中具有较多的胡萝卜素,它是人体的主要营养之一。α-胡萝卜素的结构为: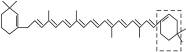
(1)写出α-胡萝卜素的分子式________。
(2)1 mol胡萝卜素最多能与________ mol Br2反应。
(3)β-胡萝卜素与α-胡萝卜素互为同分异构体,且只是虚线框内部分不同,但碳的骨架相同,写出β-胡萝卜素方框内可能的结构简式:______________________。
A、B两种烃通常状况下均为气态,它们在相同状况下的密度之比为1∶3.5。若A完全燃烧,生成CO2和H2O的物质的量之比为1∶2,则A的分子式是________,B的分子式是________。
某烃A 0.2 mol在O2中充分燃烧时,生成化合物B、C各1.2 mol。试完成下列问题:
(1)烃A的分子式为________,B、C的分子式分别是________,________。
(2)若一定量的烃A燃烧后生成B和C各3 mol,则有________g烃A参加了反应,燃烧时消耗标准状况下O2________L。
(3)若烃A不能因反应而使溴水褪色,在一定条件下能与Cl2发生取代反应,其一氯代物只有一种,则烃A的结构简式为___________。
有一平均相对分子质量为30.4的CO、C2H4和O2的混合气体,经点燃完全反应后,测得反应后混合气体中不再有CO和C2H4。试通过计算填空:
(1)原混合气体中氧气所占的体积分数为__________。
(2)原混合气体中一氧化碳的体积分数(用x表示)的取值范围为(用百分比表示)__________。
(3)原混合气体中乙烯的体积分数(用y表示)的取值范围为(用百分比表示)__________。
某烃相对分子质量为84,该烃可使溴水褪色,且分子内的碳原子都在同一平面上,则此烃的结构简式为_________,名称为_________。