ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2: 2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+ 2CO2↑+2H2O 下列说法不正确的是 ( )
2CO2↑+2H2O 下列说法不正确的是 ( )
| A.KClO3在反应中得到电子 | B.ClO2是还原产物 |
| C.H2C2O4在反应中被氧化 | D.1 molKClO3参加反应有2mol电子转移 |
氮化钠和氢化钠都是离子化合物,与水反应的化学方程式(未配平)如下:Na3N+H2O→NaOH+NH3,NaH+H2O→NaOH+H2。有关它们的叙述 ①与水反应都是氧化还原反应;②与水反应后的溶液都显碱性;③与盐酸反应都只生成一种盐;④两种化合物中的阴阳离子均具有相同的电子层结构。其中正确的是
| A.①②③④ | B.①②③ | C.②③ | D.② |
用下列实验装置和方法进行相应实验,能达到实验目的的是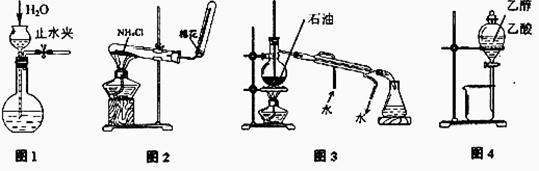
| A.用图1所示方法检查装置的气密性 |
| B.用图2所示装置和方法制取氨气 |
| C.用图3所示装置和方法进行石油分馏 |
| D.用图4装置和方法分离乙醇与乙酸 |
在一无色溶液中检验出有Ba2+、Ag+,同时又测得其酸性很强。某学生还要鉴定此溶液中是否大量存在:①Cu2+②Fe3+③ Cl-④ NO3-⑤S2-⑥CO32-⑦ NH4+⑧Mg2+⑨Al3+⑩AlO2-离子。其实,这些离子中有一部分不必再鉴定就能加以否定,你认为不必鉴定的离子组是
| A.③⑤⑥⑦⑩ | B.①②⑤⑥⑧⑨ | C.③④⑦⑧⑨ | D.①②③⑤⑥⑩ |
下列关于有机物的说法正确的是
| A.棉花、羊毛、蚕丝均属于天然纤维素 |
| B.石油的分馏和裂化均属于化学变化 |
| C.油脂都不能使溴的四氯化碳溶液褪色 |
| D.甲烷、乙醇、乙酸在一定条件下都能发生取代反应 |
下列表示化学反应的离子方程式,其中正确的是
| A.NaAlO2溶液中滴加过量盐酸:AlO2-+H2O+H+= AI(OH)3 |
B.NH4HSO3溶液与足量浓NaOH溶液共热:NH4++HSO3-+2OH- NH3↑+SO32-+H2O NH3↑+SO32-+H2O |
C.明矾溶于水产生Al(OH)3胶体: Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
| D.FeCl3溶液与Cu反应:Fe3++Cu = Fe2++ Cu2+ |