某物质A在一定条件下加热分解,产物都是气体。分解方程式为2A=B+2C+2D。测得生成物的混合气体对氢气的相对密度为d,则A的式量为( )
A.7d B.5d C.2.5d D.2d
下列各组中的两物质相互反应时,与反应条件和用量无关的是
| A.Na和O2 | B.Fe和FeCl3 |
| C.CO2和NaOH | D.AlCl3和NaOH |
下列物质中,既能和酸反应又能和碱反应的化合物是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
| A.②③④ | B.①②④ | C.①②③④ | D.①③④ |
除去NaCl溶液中混有的Ca2+、Mg2+、SO42-、HCO3-等杂质,通常采用以下四种试剂:①Na2CO3 ②BaCl2 ③NaOH ④盐酸,加入试剂顺序合理的是
| A.④②①③ | B.①③②④ | C.③②①④ | D.①②③④ |
实验是研究化学的基础,下图中所示的实验方法、装置或操作均正确的是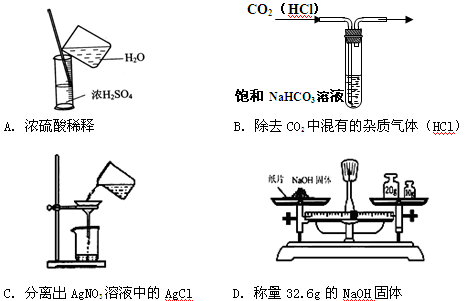
“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质
①是溶液 ②是胶体 ③是浊液 ④不能透过滤纸 ⑤能透过滤纸
⑥ 能产生丁达尔效应 ⑦静置后,会析出黑色沉淀
| A.②⑤⑥ | B.②⑥⑦ | C.①⑤ | D.③④⑦ |